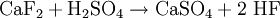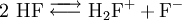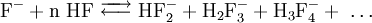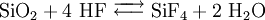Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Fluorwasserstoff
Fluorwasserstoff ist ein anorganisch-chemischer Stoff und gehört zu den Halogenwasserstoffen. Bei Zimmertemperatur liegt es als farbloses, stechend riechendes Gas vor, das leichter als Luft ist. Es ist hygroskopisch und dehydratisiert viele Stoffe. In der wasserfreien Form liegt es unterhalb des Siedepunktes von 19,51 °C als rauchende Flüssigkeit vor. Fluorwasserstoff ist in jedem Verhältnis mit Wasser mischbar und reagiert dabei sauer. Die wässrige Lösung ist als Fluorwasserstoffsäure oder Flusssäure bekannt. Entdeckt wurde die Fluorwasserstoff-Synthese aus den Elementen durch Henri Moissan. Produkt-Highlight
Gewinnung und DarstellungHeutzutage wird Fluorwasserstoff durch die Reaktion seiner Salze, den Fluoriden (Beispiel: Calciumfluorid, Flussspat), mit konzentrierter Schwefelsäure hergestellt: Anwendung findet diese Reaktion auch beim Nachweis von Fluoriden mittels der Kriechprobe. Achtung: Aufgrund der starken Reizwirkung von Fluorwasserstoff sollten alle Versuche, bei denen dieser auch nur in geringsten Mengen freigesetzt wird, im Abzug durchgeführt werden! Fluorwasserstoff fällt außerdem bei der Aluminiumherstellung und beim Brennen von Ziegeln und Feinkeramik an. Weiterhin wird es bei der Verbrennung von fluorhaltigen Abfällen oder Brennstoffen wie beispielsweise Steinkohle freigesetzt. EigenschaftenPhysikalische Eigenschaften
Chemische EigenschaftenDas chemische Verhalten des Fluorwasserstoffs wird geprägt durch die extrem hohe Elektronegativität des Fluors, welches mit 4 (Pauling-Skala) die höchste aller Elemente aufweist. Das Fluorwasserstoffmolekül ist gekennzeichnet durch einen ausgeprägten Dipolcharakter mit starker negativer Partialladung beim Fluor-Atom. Durch Wasserstoffbrückenbindungen bilden sich Polymere wie etwa H6F6. Der unter Halogenwasserstoffen relativ hohe Siedepunkt von 19,51 °C, HCl siedet beispielsweise schon bei -85,05 °C, ist wie beim Wasser auf diese Bindungskräfte zurückzuführen. Während die wässrige Lösung, die Flusssäure, nur eine schwache Säure ist, so ist wasserfreier Fluorwasserstoff eine der stärksten bekannten Brönsted-Säuren und dissoziert folgendermaßen: Fluorwasserstoff ätzt Glas und reagiert mit anderen Silikaten zu gasförmigem Silicumtetrafluorid: Fluorwasserstoff zeigt innerhalb der Reihe der Halogenwasserstoffe die schwächste Neigung zur Dissoziation in Wasser. Gegenüber den übrigen Halogenwasserstoffen, die vollständig dissoziieren unter Bildung von Oxonium-Ionen (H3O+) und ihrer entsprechenden Gegenionen, liegt in der Flusssäure ein Gemisch verschiedener fluoridhaltiger Ionen vor. Reines gasförmiges Fluorwasserstoff kann in Tankwaggons aus Eisen transportiert werden. Denn die Oberfläche des Eisen überzieht sich mit einer Fluoridschicht, die das Material gegen weiteren Angriff passiviert. Für Ventile, Rohrleitungen und Apparaturen wird auch Monelmetall (eine Nickel-Kupfer-Legierung) verwendet. Die wässrigen Lösungen dagegen würden das Eisen aufgrund des Anlösen der Fluoridschicht tiefgreifend oxidieren. Daher wird Flusssäure in Kunststoff-Tanks transportiert. VerwendungFluorwasserstoff findet Verwendung bei der Herstellung von Fluorkohlenwasserstoffen, Aluminiumfluorid, synthetischem Kryolith (Eisstein, Na6[AlF6]), Uranhexafluorid, anderen Fluorverbindungen, Flusssäure, beim Herstellungsprozess von Tensiden und in der Farbstoffchemie. Bei der Elektrolyse von Fluorwasserstoff entsteht unter bestimmten Bedingungen elementares Fluor (F2). Fluorwasserstoff wird als Katalysator bei der Benzinherstellung, als Lösungsmittel, in der organischen Chemie für die Substitution mit Fluor und in der Tieftemperaturtechnik eingesetzt. Biologische BedeutungDer Hauptaufnahmeweg für Fluorwasserstoff verläuft über die Atemwege und über die Haut. Aufgrund der hohen Hygroskopizität dürfte es nur in Extremfällen zum Einatmen von gasförmigem Fluorwasserstoff kommen, bei der aber mit nahezu vollständiger Resorption in den oberen Atemwegen zu rechnen ist. Viel häufiger tritt die Resorption von wässrigen Lösungen von Fluorwasserstoff (Fluorwasserstoffsäure oder Flusssäure) über die Haut auf. Die Haut stellt bei der Aufnahme kein Hindernis dar. Mit einer versehentlichen oralen Aufnahme ist aus physikalisch-chemischen Gründen und wegen des äußerst stechenden Geruches nicht zu rechnen. Wässrige Lösungen werden vollständig resorbiert. Der Vorgang kann durch eventuellen Mageninhalt verlangsamt werden. Kontakt mit Fluorwasserstoff hat akut stark ätzende Wirkung auf Haut und Schleimhäute, insbesondere des Auges. Durch Aufnahme in den Organismus kommt es zur erheblichen Beeinflussung biochemischer Stoffwechselvorgänge durch Enzymhemmung. Chronische Auswirkungen umfassen die Schädigung des Skeletts und der Haut, sowie Beeinträchtigung der Lungenfunktion. SicherheitshinweiseErste-Hilfe-MaßnahmenAugenNach Kontakt mit Flüssigkeitsspritzern oder Dämpfen von Fluorwasserstoff sofort mit sehr viel Wasser sehr lange spülen. Dabei das evtl. nicht verletzte, andere Auge schützen. Anschließend sofortiger Transport zum Augenarzt. HautEs ist in jedem Falle eine 20–30-minütige Spülung mit Wasser erforderlich – auch nach Einwirkung von Dämpfen. Danach Calciumgluconat-Gel reichlich auftragen und einmassieren. Nach großflächigem Kontakt – z. B. nach Aufenthalt in einer stark fluorwasserstoffhaltigen Atmosphäre ohne spezifischen Körperschutz – sollte sich der Verunfallte sofort (bei belassenem Atemschutz) unter die Schwalldusche stellen und sich erst während des Duschens entkleiden (Atemschutz zuletzt entfernen). Helfer müssen auf Selbstschutz achten! Nach gründlicher Spülung Kompressen auflegen, die mit 20 %iger Calciumgluconatlösung getränkt sind. Zwischenzeitlich Notarzt rufen! In allen Fällen eines Kontaktes mit wasserfreiem Fluorwasserstoff ist mit einer zusätzlichen massiven inhalativen Exposition, die besonderer Erste-Hilfe-Maßnahmen (s. u.) bedarf, unbedingt zu rechnen! AtmungsorganeVerletzten unter Selbstschutz aus dem Gefahrenbereich an die frische Luft bringen. Ehestmöglich ein Glucocorticoid-Dosieraerosol zur Inhalation wiederholt tief einatmen lassen. Bei Atemnot Sauerstoff inhalieren lassen. Verletzten ruhig lagern, vor Unterkühlung schützen. Bei Atemstillstand Mund-zu-Nase-Beatmung, falls nicht durchführbar Mund-zu-Mund-Beatmung. Atemwege freihalten. Zwischenzeitlich Arzt zur Unfallstelle rufen. VerschluckenMund ausspülen, Flüssigkeit wieder ausspucken. Sofort - bei erhaltenem Bewusstsein - reichlich Flüssigkeit (Wasser) trinken lassen. Erbrechen nicht anregen. Für ärztliche Behandlung sorgen. QuellenKategorien: Giftiger Stoff | Ätzender Stoff | Fluorverbindung | Wasserstoffverbindung | Fluorid |
||||||||||||||||||||||||||||||||||||||||||||||||||
| Dieser Artikel basiert auf dem Artikel Fluorwasserstoff aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. | ||||||||||||||||||||||||||||||||||||||||||||||||||