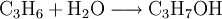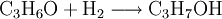Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
2-Propanol
2-Propanol, auch als Isopropylalkohol oder Isopropanol (abgekürzt IPA) bekannt, ist der kleinste nicht-cyclische, sekundäre Alkohol. Produkt-Highlight
Physikalische EigenschaftenIsopropanol ist eine schnell verdunstende, farblose, brennbare Flüssigkeit, die einen leicht süßlich-angenehmen, bei stärkerem Einatmen jedoch stechenden Geruch besitzt – dieser ist charakteristisch und erinnert an Krankenhäuser und Arztpraxen, da Isopropanol Bestandteil vieler Desinfektionsmittel ist. Isopropanol ist mit Wasser in jedem Verhältnis homogen mischbar und bildet ein konstant siedendes (azeotropes) Gemisch bei 80,4 °C und 12,1 % Wasseranteil.
Toxikologische EigenschaftenDie Dämpfe wirken betäubend. Der Kontakt verursacht Reizungen der Augen und der Schleimhäute. Beim Umgang für ausreichende Lüftung sorgen. In Tierversuchen wurden keine Hinweise auf sensibilisierende oder mutagene Eigenschaften gefunden. HerstellungDie großtechnische Herstellung erfolgt auf zwei verschiedenen Wegen, ausgehend von Propen oder von Aceton. Die Herstellung aus Propen erfolgt durch Hydratisierung an sauren Ionentauscherharzen als Katalysator: Ausgehend von Aceton erfolgt die Herstellung von Isopropanol durch Hydrierung: Durch Umkehrung dieser Reaktion wird großtechnisch Aceton aus Isopropanol durch Oxidehydrierung erzeugt, d. h. Dehydrierung mit gleichzeitiger Oxidation des entstandenen Wasserstoffs mit Sauerstoff zu Wasser. Verwendung
Sicherheit2-Propanol kann, wie andere sekundäre Alkohole auch[2], mit Luftsauerstoff explosionsfähige Peroxide bilden.[3][4][5] In zehn Jahre alten Originalgebinden von Isopropanol wurde beispielsweise ein Peroxidgehalt von 1% festgestellt. Peroxid-Konzentrationen bis 4,2% wurden berichtet.[2] Beim Abdestillieren von IPA bis zur Trockene ist es deshalb zu teils schweren Unfällen gekommen. Es ist deshalb ratsam IPA vor dem Abdestillieren auf Peroxide zu prüfen. Quellen
Kategorien: Feuergefährlicher Stoff | Reizender Stoff | Alkohol |
||||||||||||||||||||||||||||||||||||||||||||||||||
| Dieser Artikel basiert auf dem Artikel 2-Propanol aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. | ||||||||||||||||||||||||||||||||||||||||||||||||||