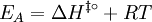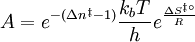Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Eyring-TheorieDie Eyring-Theorie[1] (nach Henry Eyring (1901-1981)) oder auch Theorie des Übergangszustandes (Transition State Theory = TST) genannt, ist eine molekulare Reaktionstheorie. Sie wurde unter Berücksichtigung molekularer Größen, der Zustandssummen, abgeleitet und beschreibt die absolute Reaktionsgeschwindigkeitskonstante einer chemischen Reaktion. Die Edukte sind von den Produkten durch einen Potentialwall (Aktivierungsbarriere) getrennt, der einen Sattelpunkt auf der Potentialhyperfläche darstellt. Die Reaktion der Edukte über den Übergangszustand zu den Produkten verläuft entlang einer Trajektorie, der Reaktionskoordinate (Weg zwischen den Edukten und Produkten mit jeweils minimaler Änderung der potentiellen Energie). Der Punkt höchster potentieller Energie auf dieser Reaktionskoordinate, ist der Übergangszustand. Den Begriff Aktivierter Komplex sollte man nicht mehr verwenden. [2] [3] Die wichtigsten Annahmen, die der TST zugrunde liegen, sind:
k = Geschwindigkeitskonstante, κ = Transmissionskoeffizient, kb = Boltzmann-Konstante, T = Temperatur, h = Planck´sches Wirkungsquantum, Produkt-Highlight
HerleitungDie Herleitung erfolgt für eine Beispielreaktion, in denen die Edukte A und B zum Produkt P reagieren. Als Zwischenstufe definiert man den Übergangszustand Die Reaktionsgeschwindigkeit wird als Produktbildungsgeschwindigkeit definiert, wobei die "Konzentration" des Übergangszustandes und die Konzentrationen von A und B ersetzt wird. Man erhält: Man fasst zusammen und bezieht die Produktbildungsgeschwindigkeit auf die Edukte A und B und erhält für die Geschwindigkeitskonstante k Die weitere Herleitung unterscheidet sich je nach Lehrbuch. Man erhält als Ergebnis die oben angegebene Eyring-Gleichung. Die Geschwindigkeitskonstante wobei der Transmissionskoeffizient κ nicht abgeleitet wird, sondern als zusätzlicher Parameter zur Anpassung von experimentellen Ergebnissen an die berechneten eingeführt wird. Häufig findet man in Lehrbüchern die Darstellung: mit
Thermodynamische FormulierungMit der van't Hoffschen Reaktionsisothermen Die Legendre-Transformation Aus der Arrhenius-Gleichung Analog kann man die Eyring-Gleichung unter Berücksichtigung der van't Hoffschen Reaktionsisobare Daraus folgt, wenn man die Definition der Enthalpie H = E + PV einsetzt (bei konstantem Druck): Für unimolekulare Reaktionen ist Bei idealen Gasen erhält man für den präexponentiellen Faktor: Kritik
Siehe auchQuellen
LiteraturKategorien: Chemische Reaktion | Kinetik (Chemie) |
|
| Dieser Artikel basiert auf dem Artikel Eyring-Theorie aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. |


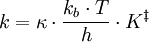
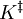 =
= 


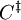 .
.
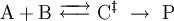
![\frac{d\mathrm{[P]}}{dt}=k^{\ddagger} \cdot \mathrm{[C^{\ddagger}]}](images/math/1/f/d/1fd3d6650c9e8145fd52f3942470e934.png)
![\mathrm{[C^{\ddagger}]}](images/math/a/e/3/ae3c056858b516986740049dfb85b999.png) durch die Gleichgewichtskonstante des vorgelagerten Gleichgewichtes
durch die Gleichgewichtskonstante des vorgelagerten Gleichgewichtes
![K^{\ddagger}=\mathrm{\frac{[C^{\ddagger}]}{[A] \cdot [B]}}](images/math/c/9/9/c99de98219bc61151d25347c9b52a8d5.png)
![\frac{d\mathrm{[P]}}{dt}=k^{\ddagger} \cdot K^{\ddagger} \mathrm{\cdot [A] \cdot [B]}](images/math/4/1/1/41124d2aebb550e02845cfdf0c7a5690.png)
![\frac{d\mathrm{[P]}}{dt}=k \mathrm{\cdot [A] \cdot [B]}](images/math/8/5/7/857e6d57167f1a0c9fee15c6769b0406.png)
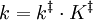
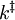 ergibt sich als
ergibt sich als
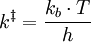
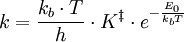
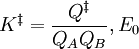 : Differenz zwischen den Nullpunktsschwingungsenergien der Edukte und des Übergangszustandes.
: Differenz zwischen den Nullpunktsschwingungsenergien der Edukte und des Übergangszustandes.
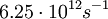 und wird als Frequenz-Faktor bezeichnet. Er liegt in der Größenordnung von Stoßfrequenzen der Moleküle in
und wird als Frequenz-Faktor bezeichnet. Er liegt in der Größenordnung von Stoßfrequenzen der Moleküle in 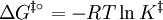 ergibt sich:
ergibt sich:
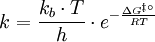
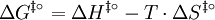 der
der 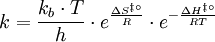
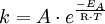 erhält man eine formale Definition für die Aktivierungsenergie
erhält man eine formale Definition für die Aktivierungsenergie 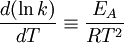
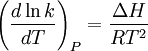 umschreiben:
umschreiben:
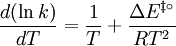
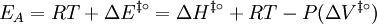
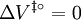 und für Reaktionen in Lösungen und
und für Reaktionen in Lösungen und