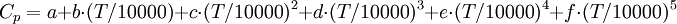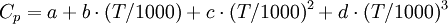Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Liste der spezifischen Wärmekapazitäten
Im NIST Chemistry WebBook findet man weitere Polynomansätze für verschiedene Stoffe (einschließlich Standard Entropie und Standard Enthalpie) Produkt-Highlight
Feststoffe
Flüssigkeiten
Temperaturabhängigkeit der "Molwärme" Cp bei WasserMit der Beziehung: können im Temperaturbereich 273 K - 473 K (0-200 °C) die Wärmekapazitäten von Wasser berechnet werden. Die Einheit [J / (mol K)] kann leicht durch Division durch die molare Masse [g/mol] in die technische Einheit [J / (g K)] umgerechnet werden.
Temperaturabhängigkeit von Cp bei Flüssigkeiten
(Anm.: die zugrundeliegenden Messdaten wurden in 5K-Schritten erfasst, Messung >100°C in druckdichter Messzelle. Bei 30–50 °C wurde eine ausgeprägte Cp-Anomalie registriert, der 25-°C-Wert ist berechnet; Parameter ergeben in die Gleichung eingesetzt keine korrekten Werte -> irgendein Parameter vertauscht?)
Gase
Temperaturabhängigkeit der "Molwärme" CpMit der Beziehung können im Temperaturbereich 273 K - ca. 1300 K (0-1000 °C) die Wärmekapazitäten von Gasen berechnet werden. Die Einheit [J/(mol K)] kann leicht durch Division durch die molare Masse [g/mol] in die technische Einheit [J/(g K)] umgerechnet werden. Die Cp-Werte für 25 °C wurden als Beispiele hiermit berechnet. (Anm.: auch über der flüssigen Phase eines Stoffs existiert eine messbare gasförmige Phase). Temperaturabhängigkeit von Cp bei Gasen
Literatur
Kategorien: Thermodynamik | Liste (Chemie) | Stoffeigenschaft |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dieser Artikel basiert auf dem Artikel Liste_der_spezifischen_Wärmekapazitäten aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. |