Die kälteste chemische Reaktion
Mit der ultrakalten Chemie erhalten Forscher einen ersten Blick darauf, was genau während einer chemischen Reaktion passiert
Anzeigen
Die kälteste chemische Reaktion im bekannten Universum fand in einem scheinbar chaotischen Durcheinander von Lasern statt. Der Schein trügt: Tief in diesem akribisch organisierten Chaos, bei Temperaturen, die Millionen Mal kälter sind als der interstellare Raum, erreichte Kang-Kuen Ni eine Höchstleistung an Präzision. Sie zwang zwei ultrakalte Moleküle, sich zu treffen und zu reagieren, und brach und bildete die kältesten Bindungen in der Geschichte der molekularen Kopplungen.
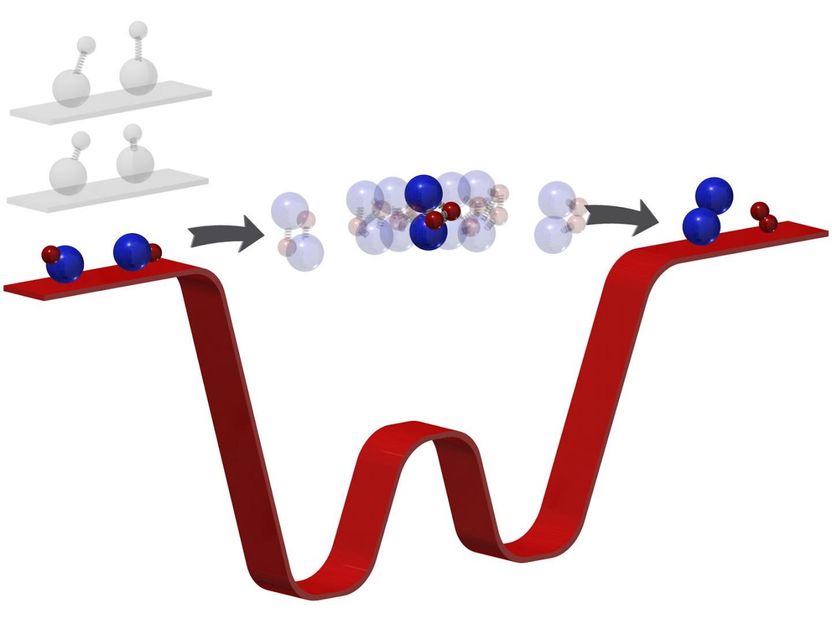
Chemische Reaktionen transformieren Reaktanden in Produkte durch einen Zwischenzustand, in dem Bindungen brechen und sich bilden. Diese Phase, die oft zu kurzlebig ist, um sie zu beobachten, entzieht sich bisher einer intimen Untersuchung. Durch das "Ausfrieren" der Rotation, Vibration und Bewegung der Reaktanden (hier Kalium-Rubidium-Moleküle) auf eine Temperatur von 500 Nanokelvin (knapp über der absoluten Nulltemperatur) wird die Anzahl der energetisch zulässigen Ausgänge für die Produkte begrenzt. "Gefangen" in der Zwischenstufe können die Forscher diese Phase dann direkt mit der Photoionisationsdetektion beobachten. Diese Technik ebnet den Weg zur Quantensteuerung chemischer Reaktionen mit ultrakalten Molekülen.
Ming-Guang Hu
"Wahrscheinlich sind wir in den nächsten Jahren das einzige Labor, das dies tun kann", sagte Ming-Guang Hu, ein Postdoc im Ni-Labor und Erstautor der in Science veröffentlichten Studie. Vor fünf Jahren machte sich Ni, der Morris Kahn Associate Professor für Chemie und Chemische Biologie und Pionier der ultrakalten Chemie, daran, ein neues Gerät zu bauen, das die chemischen Reaktionen bei niedrigsten Temperaturen aller derzeit verfügbaren Technologien erreichen konnte. Aber sie konnten nicht sicher sein, ob ihre komplizierte Technik funktionieren würde.
Jetzt haben sie nicht nur die kälteste Reaktion ausgeführt, sondern auch entdeckt, dass ihr neues Gerät etwas bewirken kann, obwohl sie es nicht vorhergesagt haben. Bei so intensiver Kälte - 500 Nanokelvin oder nur ein paar Millionstel Grad über dem absoluten Nullpunkt - konnten Ni und ihr Team etwas sehen, was noch niemand zuvor gesehen hatte: den Moment, in dem sich zwei Moleküle zu zwei neuen Molekülen treffen. Im Wesentlichen haben sie eine chemische Reaktion in ihrem kritischsten und schwer fassbaren Akt eingefangen.
Chemische Reaktionen sind buchstäblich für alles verantwortlich: Atmen, Kochen, Verdauen, Energieerzeugung, Arzneimittel und Haushaltsprodukte wie Seife. Wenn man also versteht, wie sie auf einer grundlegenden Ebene funktionieren, könnte es den Forschern helfen, Kombinationen zu entwerfen, die die Welt noch nie gesehen hat. Mit einer nahezu unendlichen Anzahl neuer Kombinationen könnten diese neuen Moleküle endlose Anwendungen finden, von einer effizienteren Energieerzeugung über neue Materialien wie schimmelfreie Wände und noch bessere Bausteine für Quantencomputer.
In ihrer früheren Arbeit nutzte Ni immer kältere und kältere Temperaturen, um diese chemische Magie zu wirken: Sie schmiedet Moleküle aus Atomen, die sonst nie reagieren würden. Auf solche Extreme abgekühlt, verlangsamen sich Atome und Moleküle zu einem Quantencrawl, ihrem niedrigstmöglichen Energiezustand. Dort kann Ni molekulare Wechselwirkungen mit höchster Präzision manipulieren. Aber auch sie konnte nur den Beginn ihrer Reaktionen sehen: Zwei Moleküle gehen rein, aber was dann? Was in der Mitte und am Ende geschah, war ein Schwarzes Loch, das nur Theorien erklären konnten.
Chemische Reaktionen laufen in nur Millionstel Milliardstel Sekunden ab, in der Wissenschaft besser bekannt als Femtosekunden. Selbst die fortschrittlichste Technologie von heute kann etwas so Kurzlebiges nicht erfassen, wenn auch nicht annähernd. In den letzten zwanzig Jahren haben Wissenschaftler ultraschnelle Laser wie Schnellaktionskameras verwendet, die schnelle Bilder von Reaktionen aufnehmen, wie sie auftreten. Aber sie können nicht das ganze Bild erfassen. "Meistens", sagte Ni, "sieht man einfach, dass die Reaktanden verschwinden und die Produkte in einer Zeit erscheinen, die man messen kann. Es gab keine direkte Messung, was tatsächlich bei diesen chemischen Reaktionen passiert ist." Bis jetzt.
Die ultrakalten Temperaturen von Ni erzwingen Reaktionen mit einer vergleichsweise gefühllosen Geschwindigkeit. "Weil die Moleküle so kalt sind", sagte Ni, "jetzt haben wir irgendwie einen Engpasseffekt." Als sie und ihr Team auf zwei Kaliumrubidiummoleküle reagierten - die aufgrund ihrer Flexibilität ausgewählt wurden - zwangen die ultrakalten Temperaturen die Moleküle, in der Zwischenstufe für Mikrosekunden zu verweilen. Mikrosekunden - wenige Millionstel einer Sekunde - mögen kurz erscheinen, aber das ist Millionen Mal länger als üblich und lang genug für Ni und ihr Team, um die Phase zu untersuchen, in der Bindungen brechen und im Wesentlichen bilden, wie ein Molekül in ein anderes übergeht.
Mit dieser intimen Vision sagte Ni, dass sie und ihr Team Theorien testen können, die vorhersagen, was in dem schwarzen Loch einer Reaktion passiert, um zu bestätigen, ob sie es richtig gemacht haben. Dann kann ihr Team neue Theorien entwickeln, indem es aktuelle Daten verwendet, um genauer vorherzusagen, was bei anderen chemischen Reaktionen passiert, selbst bei solchen, die im mysteriösen Quantenreich stattfinden.
Bereits jetzt erkundet das Team, was sie in ihrem ultrakalten Prüfstand noch lernen können. Als nächstes könnten sie beispielsweise die Reaktanden manipulieren und sie aufregen, bevor sie reagieren, um zu sehen, wie sich ihre erhöhte Energie auf das Ergebnis auswirkt. Oder sie könnten sogar die Reaktion beeinflussen, wie sie stattfindet, indem sie das eine oder andere Molekül anstoßen. "Mit unserer Kontrollierbarkeit ist dieses Zeitfenster lang genug, wir können testen", sagte Hu. "Jetzt, mit diesem Gerät, können wir darüber nachdenken. Ohne diese Technik, ohne dieses Papier können wir nicht einmal darüber nachdenken."
Hinweis: Dieser Artikel wurde mit einem Computersystem ohne menschlichen Eingriff übersetzt. LUMITOS bietet diese automatischen Übersetzungen an, um eine größere Bandbreite an aktuellen Nachrichten zu präsentieren. Da dieser Artikel mit automatischer Übersetzung übersetzt wurde, ist es möglich, dass er Fehler im Vokabular, in der Syntax oder in der Grammatik enthält. Den ursprünglichen Artikel in Englisch finden Sie hier.