Maschinelles Lernen knackt Rätsel der Quantenchemie
Techniken der künstlichen Intelligenz berechnen genau die Energie, die benötigt wird, um einfache Moleküle herzustellen - oder zu brechen
Anzeigen
Ein neues Machine-Learning-Tool kann die Energie, die benötigt wird, um ein Molekül herzustellen - oder zu brechen -, mit höherer Genauigkeit berechnen als herkömmliche Methoden. Während das Tool derzeit nur einfache Moleküle bearbeiten kann, ebnet es den Weg für zukünftige Erkenntnisse in der Quantenchemie.
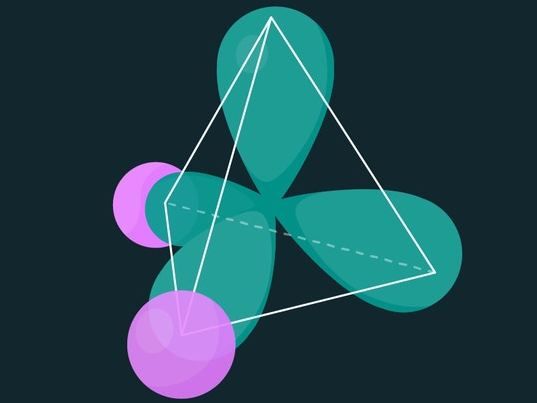
Die tetraedrische elektronische Verteilung eines Wassermoleküls. Der Sauerstoffatomkern befindet sich im Zentrum des Tetraeders, und die Wasserstoffkerne befinden sich in der Mitte der rosa Kugeln.
Simons Foundation
"Der Einsatz des maschinellen Lernens zur Lösung der fundamentalen Gleichungen der Quantenchemie ist seit mehreren Jahren ein offenes Problem, um das es im Moment viel Aufregung gibt", sagt Mitschöpfer Giuseppe Carleo, ein Forscher am Zentrum für Computational Quantum Physics des Flatiron-Instituts in New York City. Ein besseres Verständnis der Bildung und Zerstörung von Molekülen, sagt er, könnte das Innenleben der lebenswichtigen chemischen Reaktionen aufdecken.
Carleo und seine Mitarbeiter Kenny Choo von der Universität Zürich und Antonio Mezzacapo vom IBM Thomas J. Watson Research Center in Yorktown Heights, New York, stellten ihre Arbeit am 12. Mai in Nature Communications vor.
Das Tool des Teams schätzt die Energiemenge, die benötigt wird, um ein Molekül wie Wasser oder Ammoniak zusammenzusetzen oder auseinander zu ziehen. Diese Berechnung erfordert die Bestimmung der elektronischen Struktur des Moleküls, die aus dem kollektiven Verhalten der Elektronen besteht, die das Molekül zusammenbinden.
Die Berechnung der elektronischen Struktur eines Moleküls ist eine heikle Angelegenheit, bei der alle potenziellen Zustände, in denen sich die Elektronen des Moleküls befinden könnten, sowie die Wahrscheinlichkeit jedes einzelnen Zustands bestimmt werden müssen.
Da Elektronen miteinander wechselwirken und quantenmechanisch miteinander verschränkt werden, können Wissenschaftler sie nicht einzeln behandeln. Mit mehr Elektronen treten mehr Verschränkungen auf, und das Problem wird exponentiell schwieriger. Genaue Lösungen gibt es nicht für Moleküle, die komplexer sind als die beiden Elektronen in einem Wasserstoffatompaar. Selbst Annäherungen kämpfen mit der Genauigkeit, wenn sie mehr als ein paar Elektronen umfassen.
Eine der Herausforderungen besteht darin, dass die elektronische Struktur eines Moleküls Zustände für eine unendliche Anzahl von Orbitalen enthält, die immer weiter von den Atomen entfernt sind. Zudem ist ein Elektron nicht von einem anderen unterscheidbar, und zwei Elektronen können nicht denselben Zustand einnehmen. Die letztere Regel ist eine Folge der Austauschsymmetrie, die bestimmt, was passiert, wenn identische Teilchen den Zustand wechseln.
Mezzacapo und Kollegen von IBM Quantum entwickelten eine Methode zur Beschränkung der Anzahl der betrachteten Orbitale und zur Durchsetzung der Austauschsymmetrie. Dieser Ansatz, der auf Methoden basiert, die für Anwendungen im Bereich der Quanteninformatik entwickelt wurden, lässt das Problem eher Szenarien ähneln, in denen Elektronen auf vorgegebene Orte, wie z.B. in einem starren Gitter, beschränkt sind.
Die Ähnlichkeit mit starren Gittern war der Schlüssel, um das Problem handhabbarer zu machen. Carleo trainierte zuvor neuronale Netze, um das Verhalten von Elektronen zu rekonstruieren, die auf die Stellen eines Gitters beschränkt sind. Durch die Erweiterung dieser Methoden konnten die Forscher Lösungen für die verdichteten Probleme von Mezzacapo abschätzen. Das neuronale Netz des Teams berechnet die Wahrscheinlichkeit für jeden Zustand. Anhand dieser Wahrscheinlichkeit können die Forscher die Energie eines bestimmten Zustands abschätzen. Das niedrigste Energieniveau, die so genannte Gleichgewichtsenergie, ist dort, wo das Molekül am stabilsten ist.
Durch die Innovationen des Teams wurde die Berechnung der elektronischen Struktur eines Grundmoleküls einfacher und schneller. Die Forscher demonstrierten die Genauigkeit ihrer Methoden, indem sie abschätzten, wie viel Energie nötig wäre, um ein Molekül aus der realen Welt auseinander zu reißen und seine Bindungen aufzubrechen. Sie führten Berechnungen für Dihydrogen (H2), Lithiumhydrid (LiH), Ammoniak (NH3), Wasser (H2O), zweiatomigen Kohlenstoff (C2) und Distickstoff (N2) durch. Für alle Moleküle erwiesen sich die Schätzungen des Teams als sehr genau, selbst in Bereichen, in denen die bestehenden Methoden Schwierigkeiten haben.
Künftig wollen die Forscher größere und komplexere Moleküle mit Hilfe ausgefeilterer neuronaler Netze angehen. Ein Ziel ist der Umgang mit Chemikalien, wie sie im Stickstoffkreislauf vorkommen, in dem biologische Prozesse auf Stickstoff basierende Moleküle auf- und abbauen, um sie für das Leben nutzbar zu machen. "Wir wollen, dass dies ein Werkzeug ist, das von Chemikern zur Bearbeitung dieser Probleme eingesetzt werden kann", sagt Carleo.
Carleo, Choo und Mezzacapo stehen mit dem maschinellen Lernen zur Lösung von Problemen in der Quantenchemie nicht allein. Die Forscher stellten ihre Arbeit erstmals im September 2019 auf arXiv.org vor. Im selben Monat veröffentlichten jeweils eine Gruppe in Deutschland und eine weitere in Googles DeepMind in London Forschungsarbeiten, die maschinelles Lernen nutzen, um die elektronische Struktur von Molekülen zu rekonstruieren.
Die beiden anderen Gruppen verwenden einen ähnlichen Ansatz, der die Anzahl der betrachteten Orbitale nicht begrenzt. Diese Einbeziehung ist jedoch rechnerisch anstrengender, ein Nachteil, der sich bei komplexeren Molekülen nur noch verschlimmern wird. Mit den gleichen Berechnungsressourcen ergibt der Ansatz von Carleo, Choo und Mezzacapo eine höhere Genauigkeit, aber die Vereinfachungen, die vorgenommen wurden, um diese Genauigkeit zu erreichen, könnten Verzerrungen einführen.
"Insgesamt handelt es sich um einen Kompromiss zwischen Verzerrung und Genauigkeit, und es ist unklar, welcher der beiden Ansätze mehr Potenzial für die Zukunft hat", sagt Carleo. "Nur die Zeit wird uns sagen, welcher dieser Ansätze auf die anspruchsvollen offenen Probleme in der Chemie hochskalierbar ist", sagt Carleo.
Hinweis: Dieser Artikel wurde mit einem Computersystem ohne menschlichen Eingriff übersetzt. LUMITOS bietet diese automatischen Übersetzungen an, um eine größere Bandbreite an aktuellen Nachrichten zu präsentieren. Da dieser Artikel mit automatischer Übersetzung übersetzt wurde, ist es möglich, dass er Fehler im Vokabular, in der Syntax oder in der Grammatik enthält. Den ursprünglichen Artikel in Englisch finden Sie hier.