Aminosäuresynthese leichtgemacht
Ein neues Herstellungsverfahren für unnatürliche Aminosäuren verspricht, das Design maßgeschneiderter Substanzen für Medizin und Industrie zu erleichtern
Anzeigen
Die Methode beruht auf einer neuartigen Verschiebung einer Stickstoffgruppe innerhalb der entstehenden Verbindung, berichtet eine Forschungsgruppe aus der Chemie im Fachblatt „Nature Chemistry“.
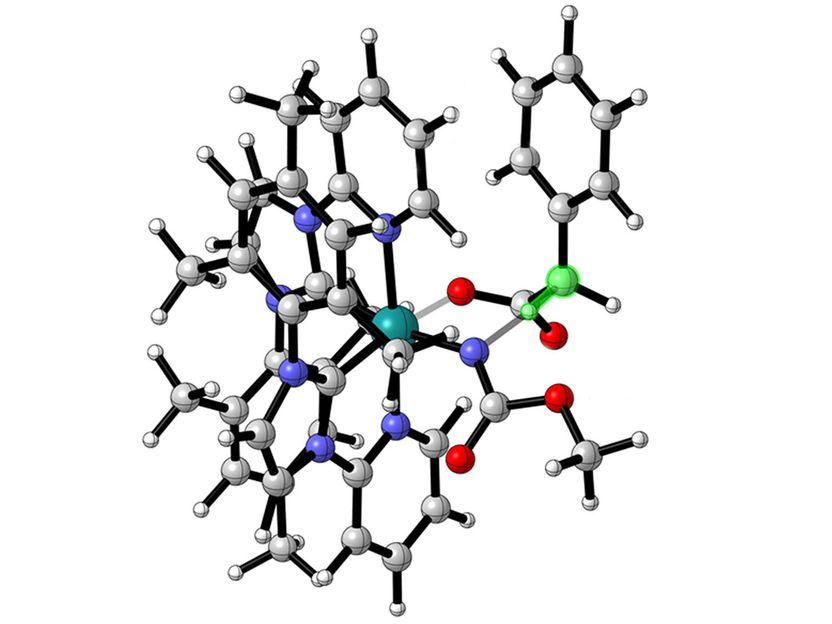
Ein Eisenkatalysator beschleunigt die Herstellung unnatürlicher Aminosäuren, hat das Team um den Marburger Chemiker Eric Meggers herausgefunden.
E. Meggers & Mitarbeiter
Proteine bestehen aus aneinander geketteten Aminosäuren. Will man Proteine an neue Zwecke in Medizin, Biotechnologie und Industrie anpassen, so kann man künstliche Aminosäuren als Kettenglieder einbauen. „Unnatürliche Aminosäuren werden auch für die Entwicklung von bioaktiven Peptiden gebraucht. Ein sehr aktuelles Beispiel ist das antivirale Medikament Paxlovid, welches von Pfizer für die Behandlung von COVID-19-Risikopatienten entwickelt wurde“, legt der Marburger Chemiker Professor Dr. Eric Meggers dar, der die Forschungsarbeit leitete.
Weltweit suchen Fachleute nach leistungsfähigen Methoden, um den steigenden Bedarf an maßgeschneiderten Aminosäuren zu decken, die in der Natur nicht vorkommen. Meggers und seine Arbeitsgruppe ließen sich von den jüngsten Fortschritten inspirieren, die mit der Stickstoffverbindung Nitren gelungen sind – einem sehr reaktionsfreudigen Molekül: Nitren drängt sich gern in Bindungen zwischen Kohlenstoff und Wasserstoff, wenn man Übergangsmetalle als Reaktionsbeschleuniger zu Hilfe nimmt. „Diese Insertion von Nitren ist ein leistungsfähiges Werkzeug, um in organische Moleküle Bindungen zwischen Stickstoff und Kohlenstoff einzuführen“, erläutert Meggers‘ Doktorand Chen-Xi Ye, einer der beiden Erstautoren des Fachaufsatzes.
Normalerweise schließt sich bei einer solchen Insertion das entstehende Molekül zu einem Ring. „Wir wollten jedoch Aminosäuren herstellen, die keinen Ring bilden – und haben das mit unserem Verfahren auch geschafft!“, berichtet Xiang Shen aus Meggers‘ Arbeitsgruppe, der sich die Erstautorenschaft mit Ye teilt. Das Stickstoffatom wechselt seinen Platz im Molekül, indem es von einem Sauerstoffatom zu einem zentralen Kohlenstoffatom übergeht.
„Unsere neue Methode ist überraschend einfach und unkompliziert“, erklärt Meggers. „Als Ausgangsmaterial verwenden wir reichlich vorhandene und leicht zugängliche Kohlenwasserstoffe, nämlich Carbonsäuren.“ Das Verfahren führe schnell zu einer Vielfalt an Aminosäuren. „Wir glauben, dass unsere Strategie die Synthese von unnatürlichen Aminosäuren enorm vereinfachen wird“, führt der Chemiker aus; „als Katalysatoren für die Stickstoffumlagerung dienen ungiftige Eisenkomplexe.“ Die Philipps-Universität Marburg hat vor Kurzem ein europäisches Patent angemeldet, das auf den Ergebnissen aus Meggers‘ Labor beruht.
Originalveröffentlichung
Weitere News aus dem Ressort Wissenschaft
Meistgelesene News
Weitere News von unseren anderen Portalen
Verwandte Inhalte finden Sie in den Themenwelten
Themenwelt Synthese
Die chemische Synthese steht im Zentrum der modernen Chemie und ermöglicht die gezielte Herstellung von Molekülen mit spezifischen Eigenschaften. Durch das Zusammenführen von Ausgangsstoffen in definierten Reaktionsbedingungen können Chemiker eine breite Palette von Verbindungen erstellen, von einfachen Molekülen bis hin zu komplexen Wirkstoffen.

Themenwelt Synthese
Die chemische Synthese steht im Zentrum der modernen Chemie und ermöglicht die gezielte Herstellung von Molekülen mit spezifischen Eigenschaften. Durch das Zusammenführen von Ausgangsstoffen in definierten Reaktionsbedingungen können Chemiker eine breite Palette von Verbindungen erstellen, von einfachen Molekülen bis hin zu komplexen Wirkstoffen.