Wenn Wasser spricht: Lösungsmittel macht Katalysatoren effizienter
Anzeigen
Warum bestimmte Katalysatormaterialien effizienter arbeiten, wenn sie von Wasser anstatt von einer Gasphase umgeben sind, ist unklar. Erste Antworten haben RUB-Chemiker nun mit Computersimulationen gewonnen. Sie zeigten, dass Wasser spezifische Ladungszustände an der Katalysatoroberfläche stabilisiert. „Katalysator und Wasser sprechen quasi miteinander“, verbildlicht Professor Dominik Marx die zugrundeliegenden komplexen Ladungstransferprozesse. Seine Arbeitsgruppe vom Lehrstuhl für Theoretische Chemie berechnete auch, wie man die Effizienz von Katalysatorsystemen ohne Wasser steigern kann, indem man Druck und Temperatur variiert.
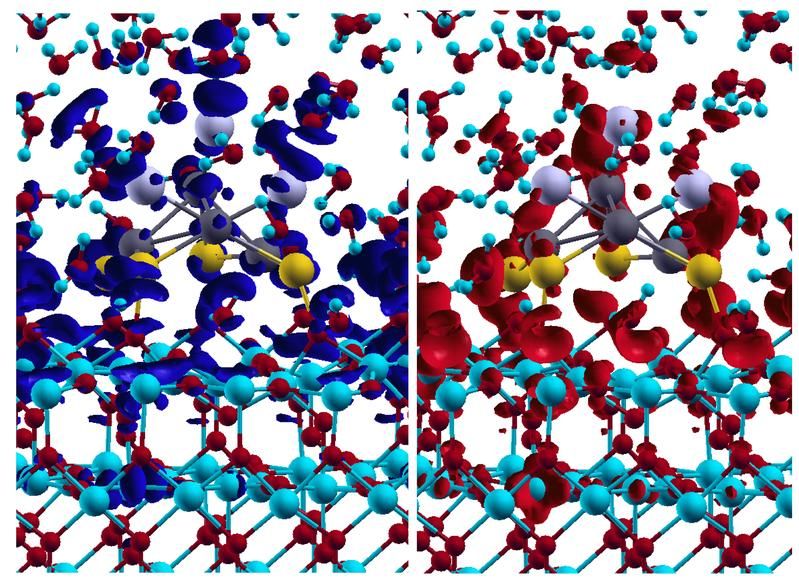
Schnappschuss des Ladungstransfers: Wasser-induzierter Ladungstransfer an der Grenzfläche zwischen Wasser und Katalysator. Die roten und blauen Flächen in dem linken bzw. rechten Bild quantifizieren die Erniedrigung bzw. Erhöhung der Elektronendichte aufgrund des Ladungstransfers zu einem bestimmten Zeitpunkt. Das blau-rote Gitter im unteren Bildteil repräsentiert das Oxid, die grauen und gelben Kugeln an der Oxidoberfläche das Metall. Die kleinen blau-roten Moleküle im oberen Bildteil sind Wassermoleküle.
M. Farnesi Camellone, D. Marx
Heterogene Katalyse: Wasser oder Gas als zweite Phase
Bei der heterogenen Katalyse kombinieren Forscher Stoffe zweier unterschiedlicher Phasen – üblicherweise fest und gasförmig. An den dadurch entstehenden Grenzflächen laufen chemische Reaktionen schneller ab als ohne Katalysator. Die Industrie nutzt die heterogene Katalyse für viele Prozesse, zum Beispiel um Alkohole in bestimmte Aldehyde umzusetzen. Als feste Phase eignet sich etwa Titandioxid mit an der Oberfläche gebundenen Goldpartikeln. Wasser – anstelle eines Gases – als zweite Phase hat mehrere Vorteile: Umweltschädliche Substanzen, die in traditionellen Verfahren zur Oxidation der Alkohole erforderlich sind, können einfach durch Luftsauerstoff ersetzt werden. Außerdem ist die ganze Reaktion in Wasser sehr effizient, auch schon bei moderaten Temperaturen.
Ladungstransfer zwischen Wasser und Katalysator
Was bei der Katalyse auf molekularer Ebene passiert, haben die theoretischen Chemiker mit sogenannten ab initio Molekulardynamik-Simulationen erforscht. Das Ergebnis: Zwischen Wasser und Katalysator findet ein Ladungstransfer statt. Elektronen, genauer gesagt Anteile von Elektronendichten, werden zwischen fester und flüssiger Phase verschoben. Auf diese Weise stabilisiere die flüssige Phase Ladungszustände an der Goldoberfläche, spekulieren die Forscher. Die Stellen, wo das passiert, könnten die aktiven Zentren des Katalysators sein, an denen die chemischen Reaktionen effizient ablaufen. Anders als Wasser kann eine Gasphase nicht auf diese Art und Weise mit dem Katalysator „sprechen“, da mit der Gasphase kein Ladungstransfer möglich ist.
Die Effizienz per Thermodynamik steigern
In einer weiteren Studie untersuchte das Team von Dominik Marx einen verwandten Metall/Oxid-Katalysator aus Kupfer und Zinkoxid, der der großindustriellen Methanolsynthese dient. Wie die Computersimulationen ergaben, ist hier vor allem das Wechselspiel zwischen fester Phase und Gasphase bedeutend für die Effizienz. Je nach Druck- und Temperaturverhältnissen bindet Wasserstoff an die Katalysatoroberfläche und stabilisiert damit indirekt katalytisch aktive Zentren, die in diesem Fall aufgrund eines Elektronentransfers zwischen Oxid und Metall entstehen. „Ohne den Wasserstoff würden die Zentren, platt gesagt, gar nicht existieren“, erklärt Marx. Die thermodynamischen Bedingungen in der Gasphase versetzen die Oberfläche auf diese Weise in einem bestimmten Zustand, der für die Arbeit des Katalysators besonders günstig ist.
Mehrwert durch Kombination
Die beiden Arbeiten zeigen also, dass sich die Katalysatoreffizienz sowohl über ein Lösungsmittel, als auch über die Thermodynamik – nämlich durch Druck und Temperatur der Gasphase – steuern lässt. Allerdings sind dafür völlig verschiedene Mechanismen verantwortlich, die die Forscher trotzdem mit den gleichen Simulationsmethoden aufklären konnten. Das macht die Ergebnisse direkt vergleichbar. In Zukunft wollen die Theoretiker mit diesen Methoden untersuchen, ob sie das Kupfer/Zinkoxid-System noch weiter optimieren können, indem sie die Gasphase durch ein geeignetes Lösungsmittel ersetzen.
Originalveröffentlichung
M. Farnesi Camellone, D.Marx. On the impact of solvation on a Au/TiO2 nanocatalyst in contact with water, The Journal of Physical Chemistry Letters, 2013.
L. Martínez-Suárez, J. Frenzel, D. Marx, B. Meyer: Tuning the reactivity of a Cu/ZnO nanocatalyst via gas phase pressure, Physical Review Letters, 2013.