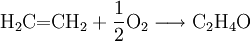Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Ethylenoxid
Ethylenoxid (kurz EO) ist ein farbloses, hochentzündliches Gas mit süßlichem Geruch und das einfachste Epoxid. Es ist ein wichtiges Zwischenprodukt bei der Herstellung von Ethylenglykol und anderen Chemikalien. Ethylenoxid wird als Desinfektionsmittel für Nahrungsmittel, organische Dämmstoffe (Wolle, Pflanzenfasern), Textilfasern und medizinische Geräte verwendet. Nach IUPAC wird es 1,2-Epoxyethan genannt. Ethylenoxid wird auch Oxiran (nach Hantzsch-Widmann-Patterson-Nomenklatur) oder Dimethylenoxid genannt. Ethylenoxid ist die UN-Nummer 1040 zugewiesen. Produkt-Highlight
GeschichteEthylenoxid wurde erstmals 1859 durch den französischen Chemiker Charles Adolphe Wurtz hergestellt, er behandelte dazu 2-Chlorethanol mit einer Base. Im Ersten Weltkrieg erlangte Ethylenoxid industrielle Bedeutung als Vorläufersubstanz für das Kühlmittel Ethylenglykol und die chemische Waffe Lost (Senfgas). 1931 entdeckte Theodore Lefort, ein anderer französischer Chemiker, die Herstellung von Ethylenoxid direkt aus Ethen und Sauerstoff mit Silber als Katalysator. HerstellungIndustriell wird Ethylenoxid durch die Umsetzung von Ethen und Sauerstoff bei 200 bis 300 °C an einem Silberkatalysator hergestellt.
Die übliche Ausbeute bei diesem Verfahren ist vom verwendeten Katalysatortyp abhängig und liegt auch in der großindustriellen Herstellung zwischen 80 und 90 %. Die parallel ablaufenden Nebenreaktionen sind die Totaloxidationen von Ethylen als auch von schon gebildetem Ethylenoxid zu CO2 und Wasser. EigenschaftenEthylenoxid ist ein hochentzündliches Gas. Der Flammpunkt beträgt −57 °C [1] und die Zündtemperatur liegt bei 435 °C [1]. Es bildet mit Luft explosionsfähige Gemische, die untere Explosionsgrenze (UEG) liegt bei 2,6 %, die obere (OEG) bei 100 % [1]. VerwendungEthylenoxidgas tötet Bakterien, Schimmel und Pilze ab, daher kann es zur Sterilisation von hitzeempfindlichen Substanzen verwendet werden. Die Sterilisation von Gewürzen mit EO wurde 1938 durch den amerikanischen Chemiker Lloyd Hall patentiert und wird heute noch verwendet. Zusätzlich wird Ethylenoxid zur Sterilisierung von Sanitätsmaterialien wie Verbänden, Nähten, Spritzen und chirurgischen Werkzeugen verwendet. Dennoch ist das meiste Ethylenoxid ein Zwischenprodukt bei der Herstellung anderer Chemikalien. Die Hauptmenge des Ethylenoxid wird für die Produktion von Ethylenglykol eingesetzt, welches ein weit verbreitetes Kühl- und Frostschutzmittel für Fahrzeuge ist. Weiter wird es für die Herstellung von Polyestern (beispielsweise PET) benötigt. Lediglich etwa 2% der Welt-Produktion wird für die Sterilisation verwendet. Ethylenoxid kann zu Polyethylenglykol (auch Polyethylenoxid) polymerisieren, welches ein ungiftiges und gut wasserlösliches Polymer ist. Es ist ebenfalls wichtig für die Herstellung von Tensiden (siehe Nichtionische Tenside). Eine Kategorie von Ethylenoxidderivaten, die große wissenschaftliche Aufmerksamkeit erregt hat, sind die Kronenether, welche zyklische Oligomere des Ethylenoxids sind. Diese Verbindungen haben die Fähigkeit, ionische Substanzen in unpolaren Lösungsmitteln löslich zu machen, in welchen sie sonst unlöslich sind. Aufgrund hoher Kosten bleibt die Verwendung dieser Substanzen auf Laboranwendungen begrenzt. GesundheitEthylenoxid ist giftig und krebserregend beim Einatmen. Symptome einer Vergiftung sind Kopfschmerzen, Schwindel und Übelkeit/Erbrechen. Mit zunehmender Dosis kommt es zu Zuckungen, Krämpfen und schlussendlich zum Koma. Es ist für die Haut und die Atemwege reizend. Die Lunge kann sich Stunden nach dem Einatmen mit Flüssigkeit füllen. Ethylenoxid wird normalerweise druckverflüssigt in Kombination mit 10 % Kohlenstoffdioxid gelagert. Bei Normaldruck und Zimmertemperatur verdunstet es sehr schnell und verursacht Frostverbrennungen auf der Haut. Labortiere, die ihr Leben lang Ethylenoxid ausgesetzt sind, haben ein höheres Risiko an Leberkrebs zu erkranken. Bei Tieren hat es zahlreiche Fortpflanzungsdefekte wie Mutationen oder Fehlgeburten ausgelöst. Der Einfluss auf die menschliche Fortpflanzung ist noch nicht genau untersucht, es gilt aber als wahrscheinlich, dass die gleichen Effekte wie im Tierversuch auftreten. Quellen
Kategorien: Feuergefährlicher Stoff | Giftiger Stoff | Heterozyklische Verbindung |
||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dieser Artikel basiert auf dem Artikel Ethylenoxid aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. | ||||||||||||||||||||||||||||||||||||||||||||||||||||