Carbon Mining: Wie Chemiker Kohlenstoff aus der Luft abbauen
Der Trick besteht darin, das CO2 am Katalysator-Material anzureichern
Anzeigen
Erstmals ist es Chemikern gelungen, unter normalen Druckverhältnissen und moderaten Temperaturen CO2 aus der Luft an einem katalytischen Material anzureichern und dort zu einer Reaktion zu bewegen. Reaktionspartner des CO2 ist Methanol, der simpelste Vertreter aus der Stoffklasse der Alkohole. Dabei entsteht Dimethylcarbonat, ein Ester der Kohlensäure, das u.a. als Kraftstoff diskutiert wird und in der Industrie giftige Chemikalien ersetzen kann. Die Reaktion gelang Forschern am Leibniz-Institut für Katalyse, Rostock.
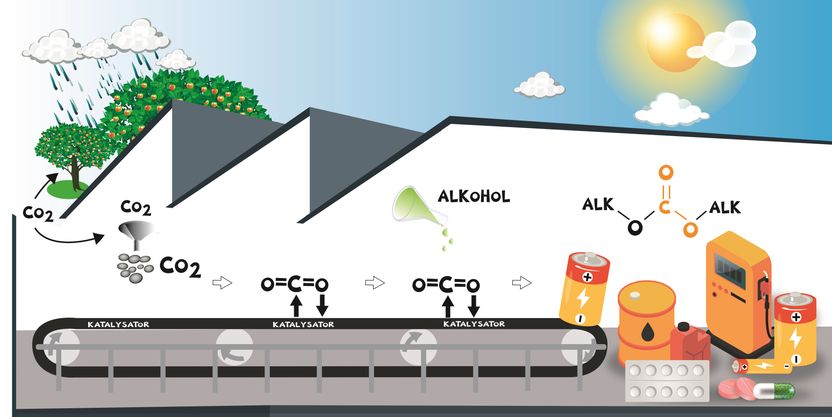
„CO2 -Ernte“ aus der Luft: An einem geeigneten Katalysator erfolgt die Anreicherung des Kohlenstoffdioxids aus der Luft und die Aktivierung des reaktionsträgen Gases. Auf diese Weise kann es direkt mit Alkoholen zu neuen Produkten umgesetzt werden.
Leibniz-Institut für Katalyse
Die Arbeiten unter Leitung von Dr. Sebastian Wohlrab ebnen den Weg zu gleich zwei großen Zielen der Chemie: zum einen Kohlendioxid direkt aus der Luft zu „ernten“ und so den Anteil des Klimagases in der Atmosphäre zu mindern. Zum anderen geht es nach den Worten von Sebastian Wohlrab um die Bereitstellung von Kohlenstoff für chemische Grundprozesse. Und zwar durch „Carbon Mining“, wie er sagt, „wenn wir einst nicht mehr in ausreichendem Maße über fossile Kohlenstoffträger – Erdöl, Erdgas und Kohle – verfügen werden“.
Essenzielles Element
Gerade die permanente Bereitstellung von Kohlenstoff ist weltweit eines der drängendsten Themen. Kohlenstoff, C, ist wie kein anderes chemisches Element in der Lage, Ringe und lange Ketten mit sich selbst zu bilden und dabei andere Elemente und Molekülgruppen für unfassbar viele Funktionen einzubinden. Auf diese Weise geht er millionenfach chemische Verbindungen ein. Diese Eigenschaft macht Kohlenstoff zum essenziellen Element. Und zwar sowohl für die Biosphäre – in Form etwa von Proteinen, Fetten und Kohlenhydraten – als auch für die industrielle Produktion.
Allerdings zählt Kohlenstoff mit einem Anteil in der Erdkruste von 0,027 Prozent zu den knappen Ressourcen. Hauptlieferant für die Industrie sind bisher Erdöl, Erdgas und Kohle. Und die Kohle- und Petrochemie wird mit wachsendem Bewusstsein für ökologisches Wirtschaften zum Auslaufmodell. Weltweit erforschen Chemiker deshalb alternative Verfahren auf der Basis nachwachsender Rohstoffe wie Holz oder Abfälle aus der Landwirtschaft, die in der Lage sind, petrochemische Großprozesse abzulösen.
Vision und Illusion
„Es ist jedoch eine große Illusion anzunehmen, die Weltwirtschaft würde ihren Bedarf an Kohlenstoff allein aus nachwachsenden Rohstoffen decken können“, sagt Sebastian Wohlrab und zitiert repräsentative Statistiken. (a) C. B. Field et al., Science 281 (5374), 237-240. b) BP Statistical Review of World Energy, 2019, 68th edition. c) FAOSTAT data on land use, 2015.) Demnach bindet das weltweite Pflanzenwachstum 56.400 Mio Tonnen elementaren Kohlenstoffs im Jahr. Und nur 14 Prozent davon, also knapp 7.900 Mio Tonnen/Jahr, werden durch Pflanzenanbau erreicht, mithin die Nahrungsgrundlage der Erdbevölkerung. Das heißt, nur diese Menge stünde für eine nachhaltige Gewinnung von Rohstoffen zur Verfügung – wenn man den Regenwald nicht vollends vernichten möchte.
Fast die gleiche Menge an Kohlenstoff, nämlich knapp 7.000 Mio Tonnen/Jahr, verarbeitet die Petrochemie derzeit weltweit zu Produkten. „Wenn wir also Erdöl und -gas durch grüne Chemie ersetzen wollen, ohne der Menschheit die Nahrungsgrundlage zu entziehen, müsste die Weltwirtschaft zu extremen Maßnahmen fähig sein“, sagt Dr. Wohlrab: Entweder den Kohlenstoffverbrauch, also die Produktion von Gütern, dramatisch zu drosseln. Oder die Fläche für den Pflanzenanbau zu verdoppeln, was ökologisch verheerend wäre. „Das verdeutlicht, wie dringend wir gänzlich andere Kohlenstoff-Quellen erschließen müssen.“ Eine Quelle davon ist das CO2 in der Atmosphäre.
Wer diese Kohlenstoff-Quelle anzapfen möchte, steht vor einer kniffligen Aufgabe, wie Sebastian Wohlrab weiter erläutert. „Der CO2-Anteil in der Luft ist mit 400 ppm für eine chemische Reaktion mit effektiven Resultaten sehr gering.“ Bisherige Verfahren zur Umsetzung von Kohlendioxid, wie die Harnstoffsynthese, nutzen hochkonzentrierte CO2-Ströme. Und die Veresterung von CO2 funktioniert im Labor bisher nur unter hohem Druck.
Mit einer Ausnahme: 2017 gelang einer chinesischen Austauschstudentin im Forschungsbereich von Sebastian Wohlrab die Esterbildung bei Atmosphärendruck – mit hochkonzentriertem Kohlendioxid. Dieses Experiment hat die Phantasie im Team von Dr. Wohlrab beflügelt. „Es lag nahe zu schauen, ob CO2 auch aus normaler Raumluft, also extrem niedrig konzentriert, umgewandelt werden kann.“
Sättigung mit Kohlendioxid
Der Trick besteht darin, das CO2 am Katalysator-Material anzureichern. Das heißt, Luft unter normalem atmosphärischen Druck solange über das Material zu leiten, bis es mit CO2 gesättigt ist. Das funktioniert, weil das Material, ein pulverförmiges Mischoxid, basische Zentren enthält. Chemiker Wohlrab: „CO2 ist ein saures Gas. Und da Gegensätze sich anziehen, reichert es sich an den basischen Zentren an.“ Die CO2-freie Abluft wird abgeführt. Ist das Katalysator-Material CO2-gesättigt, wird Methanol zugesetzt, und alles zusammen reagiert zu Dimethylcarbonat. Und zwar bei 90 Grad Celsius, für Chemiker eine moderate Temperatur.
Noch zieht sich der Prozess der CO2-Anreichung und Umsetzung mit Methanol über dreieinhalb Stunden hin. „Das dauert für ein technisches Verfahren entschieden zu lange“, sagt Dr. Wohlrab. „Die Produkt-Ausbeute ist aber bereits jetzt richtungsweisend.“ So werden drei von vier der adsorbierten CO2 Moleküle erfolgreich umgesetzt.
„Das Prinzip funktioniert. Wir haben gezeigt, dass wir Kohlenstoff aus der Luft gewinnen und ein Klimagas als Rohstoff nutzen können.“ Die Forscher kennen die Stellschrauben, an denen sie nun drehen müssen, um die Reaktion zu optimieren. Und Dr. Wohlrab vermutet, dass nach diesem Prinzip auch andere Reaktionen mit atmosphärischem CO2 möglich werden.

































































