Radikal in der Blackbox
Chemiker lüften Betriebsgeheimnis eines Katalysators
Anzeigen
Forscher am Rostocker Leibniz-Institut für Katalyse konnten bei einer Redoxreaktion die molekulare Arbeitsweise des Katalysators beobachten und wichtige Zwischenschritte aufklären. Zu diesem Zweck koppelten sie, erstmals weltweit, vier hochmoderne Messmethoden miteinander, die in unterschiedlichen Bereichen von Wellenlängen arbeiten: mit Infrarot-, UV- und Röntgenstrahlen sowie mit Mikrowellen im magnetischen Feld. Sie deckten auf diese Weise den kompletten katalytischen Mechanismus für die selektive Oxidation von Benzylalkohol zu Benzaldehyd auf. Als Grundchemikalie wird Benzaldehyd, das intensiv nach Bittermandel riecht, vor allem für Parfums und Kosmetik gebraucht.

Blick in ein EPR-Spektroskop im Forschungsbreich "Ktalytische in situ-Studien" von Prof. Angelika Brückner
LIKAT/Nordlicht
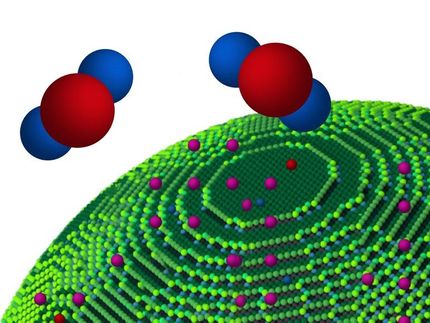
Wie so oft in der Chemie läuft auch diese Reaktion quasi in einer Blackbox ab. Ausgangsstoffe, Katalysator und Lösungsmittel kommen in ein Reaktionsgefäß und reagieren dort zum gewünschten Produkt, dem Benzaldehyd. So viel ist klar: Der Katalysator ermöglicht durch seine Anwesenheit diesen Prozess oder beschleunigt ihn zumindest. Doch welche seiner Komponenten in welcher Reihenfolge die Ausgangsstoffe aktivieren, welche reaktiven Zwischenprodukte dabei entstehen und in welcher Weise sie die Reaktion beeinflussen – das bleibt im Dunkel.
Umweltfreundliches Oxidationsmittel
Diese Informationen sind jedoch für ein gezieltes Katalysatordesign essenziell. Für die Oxidation zu Benzaldehyd verwendet die Industrie üblicherweise Oxidationsmittel, wie Chromat oder Hypochlorid, die für die Umwelt problematisch und aufwendig zu entsorgen sind. Im Labor experimentieren Forscher deshalb weltweit mit Sauerstoff, O2, als eleganterem Oxidationsmittel, bekommen allerdings, was etwa die Ausbeute betrifft, nur unzureichende Resultate. Ziel ist es also, den Katalysator zu verbessern, wozu es am besten ist, ihn sozusagen bei der Arbeit genauestens zu beobachten.
Das ist die Spezialität von Prof. Dr. Angelika Brückner, Leiterin des Forschungsbereichs „Katalytische In-situ-Studien“ und ihres Themenleiters Dr. Jabor Rabeah. Sie regen dazu Proben mit Strahlung unterschiedlicher Energie und Wellenlänge an. Durch spezifische Absorptionen aller beteiligten Spezies lassen sich Rückschlüsse auf ihre Eigenschaften, wie Oxidationsstufen oder Bindungssituationen, und somit auch auf ihre Funktion und Rolle im chemischen Prozess ziehen.
Hochkomplex und simultan
Herzstück der untersuchten Redoxreaktion ist ein Kupferkomplex, der von einem organischen Liganden, gewissermaßen der Rüstung des Katalysators, stabilisiert wird. Zum Katalysator gehört ebenfalls ein Hilfsstoff, in diesem Falle ein Radikal namens TEMPO, eine Bezeichnung, die sich aus dem Akronym seiner chemischen Struktur ableitet: TEtramethylPiperidinylOxyl.
Der Katalysator besteht also aus drei Komponenten, hinzu kommen der Ausgangsstoff und das Oxidationsmittel O2. Solch einem „komplexen System“, wie Brückner und Rabeah sagen, nähern sie sich am besten mit mehreren unterschiedlichen Methoden. Die Hürde dabei war, dass diese Messungen im selben Reaktionsgefäß, im selben Experiment, d.h. simultan, erfolgen müssen. Angelika Brückner: „Nur so können wir identische Versuchsbedingungen garantieren. Die Analysen einzeln und nacheinander vorzunehmen, ist immer mit gewissen Unterschieden in den Reaktionsbedingungen verbunden, was die Vergleichbarkeit der Ergebnisse erschweren würde.“
Die Forschenden wählten für die parallelen Messungen zunächst Infrarot- und etwas energiereichere UV-Strahlen sowie die Elektronen-Paramagnetische-Resonanz (EPR-Spektroskopie), die ungepaarte Elektronen erfasst. Zu klären war zum Beispiel die Rolle des Hilfsstoffs TEMPO, der solch ein ungepaartes Elektron aufweist – was ihn zum einen hochreaktiv macht und zum anderen die Bezeichnung als „Radikal“ einbringt.
Kooperation mit SOLEIL, Paris
Tatsächlich konnten die Wissenschaftler bei ihren ersten Messungen erkennen, dass TEMPO in die Reaktion eingreift. Doch auf welche Weise? Wenn die Reaktion startet, verändert ein Teil der Kupferpartikel seine Wertigkeit von Cu-I in Cu-II. Bisher ging die Fachwelt zumeist davon aus, dass die Cu-II-Spezies während der Reaktion eine Verbindung als sogenanntes Dimer eingeht und dass TEMPO vor allem für Oxidation des Cu-I zu Cu-II verantwortlich ist.
Um diese Vermutungen aufzuklären, benötigten die Rostocker Chemiker einen präziseren Blick auf die Kupfer-Komponenten, und zwar mit einem hochenergetischen Röntgenstrahl. Dazu kooperierten sie mit dem Synchrotron SOLEIL in Paris. Zunächst erwarben sie ein kompaktes EPR-Spektrometer, das sie durch geschickte Modifizierung der Messzelle mit einer IR- und einer UV-Sonde komplettierten. Zudem passten sie es konstruktiv für die Versuchsanordnung am Synchrotron an.
Mit vier derart ultrascharfen Sehhilfen bewaffnet konnten die LIKAT-Forscher am SOLEIL in Paris erstmals ein und denselben Prozess aus mehreren Perspektiven simultan beobachten. „Und wir konnten endlich aufklären, was in der Fachliteratur bisher kontrovers diskutiert wurde“, sagt Dr. Rabeah.
Modellreaktion für künftige Analysen
Sie entdeckten, dass TEMPO dabei gar nicht selbst oxidiert wird, wie bisher angenommen. Stattdessen aktiviert es das Oxidationsmittel Sauerstoff. Außerdem konnten sie zwar das vieldiskutierte Dimer tatsächlich nachweisen. Sie fanden aber, dass es sich im Laufe der Reaktion wieder in Monomere spaltet. Prof. Brückner: „Das aber hat keinerlei Einfluss auf die Reaktivität des Systems. Demzufolge spielt dieses Dimer für die Reaktion keine Rolle.“
Mit den Erkenntnissen kann die Fachwelt nun die Oxidation von Benzylalkohol mittels Sauerstoff weitertreiben und vor allem optimieren. Langfristig laufen diese Arbeiten darauf hinaus, den industriellen Prozess durch einen umweltfreundlichen zu ersetzen. Und wie Jabor Rabeah betont, lässt sich die neue Kopplungstechnik auch für mechanistische Analysen anderer Reaktionen nutzen – bis hin zu Stoffwechselvorgängen in lebenden Organismen.
Originalveröffentlichung
Weitere News aus dem Ressort Wissenschaft
Meistgelesene News
Weitere News von unseren anderen Portalen
Verwandte Inhalte finden Sie in den Themenwelten
Themenwelt Spektroskopie
Durch die Untersuchung mit Spektroskopie ermöglicht uns einzigartige Einblicke in die Zusammensetzung und Struktur von Materialien. Von der UV-Vis-Spektroskopie über die Infrarot- und Raman-Spektroskopie bis hin zur Fluoreszenz- und Atomabsorptionsspektroskopie - die Spektroskopie bietet uns ein breites Spektrum an analytischen Techniken, um Substanzen präzise zu charakterisieren. Tauchen Sie ein in die faszinierende Welt der Spektroskopie!

Themenwelt Spektroskopie
Durch die Untersuchung mit Spektroskopie ermöglicht uns einzigartige Einblicke in die Zusammensetzung und Struktur von Materialien. Von der UV-Vis-Spektroskopie über die Infrarot- und Raman-Spektroskopie bis hin zur Fluoreszenz- und Atomabsorptionsspektroskopie - die Spektroskopie bietet uns ein breites Spektrum an analytischen Techniken, um Substanzen präzise zu charakterisieren. Tauchen Sie ein in die faszinierende Welt der Spektroskopie!