Neuartige hybride Nanokäfige für schnellere Katalyse
Hybride Bio-Nanokäfige könnten Reaktionen zur Gewinnung industriell wichtiger Produkte effektiv katalysieren
Anzeigen
Ein neuartiger hybrider Ferritin-Nanokäfig mit Histidinresten zeigt eine 1,5-mal höhere Metallionenaufnahme und eine verbesserte katalytische Effizienz bei der Alkoholproduktion, so Forscher der Tokyo Tech in einer neuen Studie. Ihre Ergebnisse deuten darauf hin, dass hybride Bio-Nanokäfige Reaktionen zur Gewinnung industriell wichtiger Produkte effektiv katalysieren könnten.
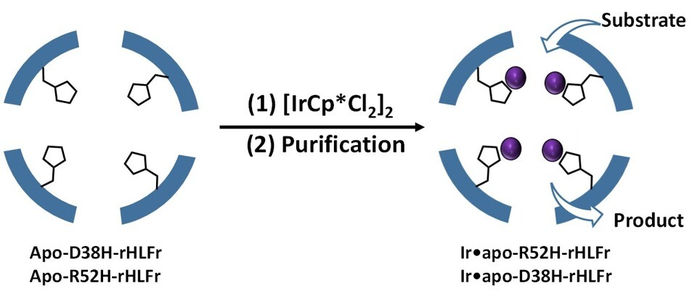
Der Käfig wurde mit Aminosäure-Ersatzstoffen ausgestattet, indem ortsspezifische Mutationen eingeführt wurden, die eine bessere Aufnahme von IrCp* ermöglichten.
Takafumi Ueno from Tokyo Institute of Technology
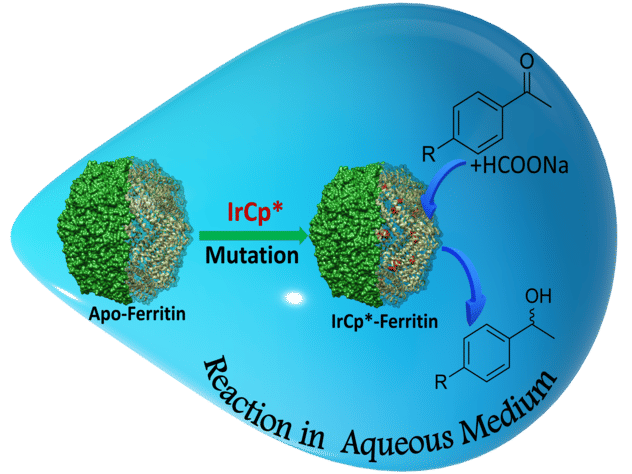
Der Nanokäfig wirkt als hybrider Biokatalysator bei der Umwandlung von Substraten in Alkohole mit hoher Spezifität.
Takafumi Ueno from Tokyo Institute of Technology
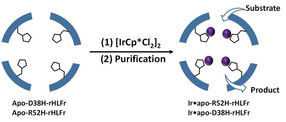
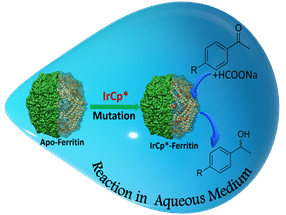
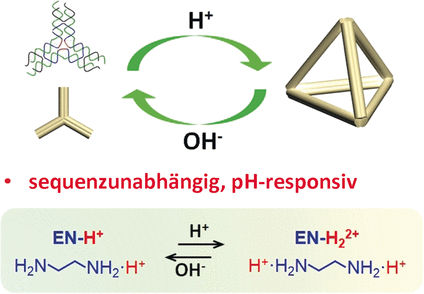
Biologische Polymere können sich spontan selbst zu komplexen Strukturen zusammenfügen, die Gefäßen oder Käfigen ähneln, aber viel kleiner sind und als "Nanokäfige" bezeichnet werden. Diese Strukturen können eine Vielzahl von Molekülen beherbergen, die sich wie "Gäste" verhalten. Ein bekanntes Beispiel ist der "Ferritin-Nanokäfig", der durch die Selbstorganisation von 24 Untereinheiten des Proteins Ferritin gebildet wird und Metallionen einschließen kann, die wichtige Katalysatoren sind. Mit Hilfe dieser Metallionen wird in einer katalytischen Reaktion ein beliebiges Substrat in ein Produkt umgewandelt. Obwohl der Ferritin-Käfig weithin bekannt ist, sind seine potenziellen Anwendungen in der Industrie noch nicht vollständig erforscht.
Bislang haben die meisten Bemühungen, die Aufnahme von Metallionen in Ferritin zu erhöhen, zu Käfigen mit geringer Stabilität geführt. Damit sich der "Gast" gut in den Käfig einfügen kann, ist ein effektives Design der Schlüssel. Vor diesem Hintergrund führte ein Team von Wissenschaftlern unter der Leitung von Prof. Takafumi Ueno vom Tokyo Institute of Technology, Japan (Tokyo Tech), ortsspezifische Mutationen im Kern des Ferritin-Nanokäfigs ein und erhöhte die Aufnahme von Iridiumkomplexen (IrCp*). Ihre Ergebnisse sind in der Zeitschrift Angewandte Chemie veröffentlicht. Iridium ist ein wichtiger Katalysator bei der Alkoholproduktion und wird in der Pharma-, Lebensmittel- und Chemieindustrie verwendet.
Prof. Ueno erklärt: "Aus der bisherigen Literatur wussten wir, dass das Vorhandensein von koordinierenden Aminosäuren im Käfig die Iridium-Aktivität verbessert, und dass der Ersatz dieser Aminosäuren durch geeignete Reste das Problem lindern könnte. Da sich der Iridiumkomplex wie ein Katalysator verhält, würden die Koordinationsreste die Aufgabe erfüllen". Die Autoren verwendeten die Aminosäure Histidin, um zwei Reste, Arginin und Asparaginsäure, der regulären Ferritin-Käfige (Wildtyp) zu ersetzen und die Mutanten R52H und D38H zu erzeugen. Bemerkenswerterweise wurden die Struktur der Baugruppe oder die Größe des Käfigs durch diese Änderungen nicht beeinträchtigt.
Als Nächstes fügten sie den Mutanten IrCp* hinzu und stellten fest, dass R52H in der Lage war, 1,5-mal mehr Iridiumatome einzubetten als der Wildtyp-Käfig. Was ihnen jedoch auffiel, war die Mutante D38H, die sich genau wie der Wildtyp verhielt! Warum hatten also nicht beide Mutationen die gleiche Wirkung? Dazu Prof. Ueno: "Das bedeutet, dass nicht nur das Vorhandensein des Histidinrests, sondern auch seine Position für die Aufnahmeeffizienz im Käfig entscheidend ist."
Mit den neuen katalytischen Käfigen konnten die Forscher eine Alkoholproduktionsrate von bis zu 88 % erreichen. Offensichtlich begünstigten die Mutationen eine strukturelle Neuanordnung der Reaktionskomponenten, was die Umwandlungsrate erhöhte.
Um zu verstehen, wie sich das Substrat im Inneren des Käfigs verhält, verwendeten die Forscher Simulationen, bei denen sich die Substratmoleküle frei im Nanokäfig bewegen konnten. Sie beobachteten einige Wechselwirkungen zwischen dem Substrat und Histidin in der R52H-Mutante, die im Wildtyp-Käfig nicht vorhanden waren, d. h. das Substrat zeigte eine bevorzugte Bindung innerhalb des Nanokäfigs.
"Diese hybriden Bio-Nanokäfige erwiesen sich auch als sehr stabil, was darauf hindeutet, dass sie als brauchbare Katalysatoren in industriellen Anwendungen eingesetzt werden könnten", schließt Prof. Ueno. Das derzeitige strukturbasierte Design der Metallionen-Bindungsstelle könnte weiterentwickelt werden, um neue Ferritin-Mutanten mit selektiver Aufnahme spezifischer Gastmoleküle für verschiedene katalytische Anwendungen in der chemischen und pharmazeutischen Industrie zu schaffen.
Hinweis: Dieser Artikel wurde mit einem Computersystem ohne menschlichen Eingriff übersetzt. LUMITOS bietet diese automatischen Übersetzungen an, um eine größere Bandbreite an aktuellen Nachrichten zu präsentieren. Da dieser Artikel mit automatischer Übersetzung übersetzt wurde, ist es möglich, dass er Fehler im Vokabular, in der Syntax oder in der Grammatik enthält. Den ursprünglichen Artikel in Englisch finden Sie hier.