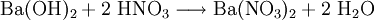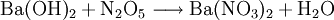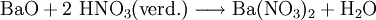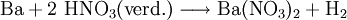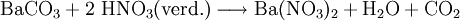Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Bariumnitrat
Bariumnitrat ist eine chemische Verbindung und ein weißer, kristalliner Feststoff. Sie ist das Barium-Salz der Salpetersäure. Produkt-Highlight
EigenschaftenDas Nitrat des Bariums ist gesundheitsschädlich und ein schwach wassergefährdender Stoff. Es verursacht in der Brennerflamme eine grüne Flammenfärbung und kann als Oxidationsmittel benutzt werden. DarstellungBariumnitrat lässt sich durch folgende chemische Reaktionen darstellen:
VerwendungBariumnitrat wird in der Pyrotechnik zur Herstellung von Feuerwerkskörpern und farbigen Wunderkerzen verwendet, weil es Flammen grün färbt und gleichzeitig ein Oxidationsmittel ist. Außerdem wird es als Oxidator in den Zündhütchen von Patronen und Kartuschen verwendet. Eine hochbrisante Mischung aus TNT und Bariumnitrat wird Baratol genannt. Es wird auch in Leuchtschirmen für Fernsehempfänger benutzt. ReaktionenBariumnitrat zersetzt sich bei Temperaturen größer 550 °C zu Bariumoxid, Stickstoff, Sauerstoff und Stickstoffmonoxid. Aufgrund des frei gesetzten Sauerstoffs ist Bariumnitrat ein gutes Oxidationsmittel. AnalytikEinen ersten Hinweis bei der Identifizierung von Barium in Bariumnitrat erhält man durch die grüne Flammenprobe. QuellenKategorien: Brandfördernder Stoff | Gesundheitsschädlicher Stoff | Nitrat | Kubisches Kristallsystem | Bariumverbindung |
||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dieser Artikel basiert auf dem Artikel Bariumnitrat aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. | ||||||||||||||||||||||||||||||||||||||||||||||||||||