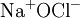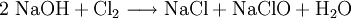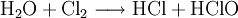Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Natriumhypochlorit
Natriumhypochlorit (NaOCl) ist das Natriumsalz der Hypochlorigen (veraltet auch Unterchlorigen) Säure (HClO). Es ist ein weißes Pulver, das im Normalfall sechs Mol Kristallwasser pro Mol Natriumhypochlorit enthält. Der Trivialname der wässrigen Lösung von Natriumhypochlorit ist Eau de Labarraque oder Eau de Javel, wobei die Bezeichnung Eau de Javel strenggenommen nicht korrekt ist. Dieses bezeichnet eine Lösung von Kaliumhypochlorit, unter Umständen in einer Mischung mit anderen Salzen wie Kaliumchlorid; wird jedoch häufig nicht unterschieden. Produkt-Highlight
Gewinnung/DarstellungNatriumhypochlorit wird durch Einleiten von Chlorgas in Natronlauge oder durch Elektrolyse einer Natriumchlorid-Lösung hergestellt. Diese Reaktion verursacht erhebliche technische Probleme. Da es sich formal um eine Hydrolyse des Chlors handelt nach mit nachfolgender Neutralisation der so entstehenden Salzsäure bzw. hypochlorigen Säure, ist leicht erkennbar, dass die Reaktionsenthalpien dieser Reaktionen zu einer starken Erwärmung führen, gegen die alle Hypochlorite empfindlich sind. Tatsächlich wird der gleiche chemische Prozess dazu verwendet, Chlorat herzustellen, jedoch durch Reaktion in heißer Lösung. Aus diesem Grunde enthalten alle technischen Hypochlorite wechselnde, manchmal große Mengen von Chlorat. Auch die Reaktion von bei der Herstellung entstandenem Hypochlorit mit Chlor führt schließlich zu Chlorat. VerwendungDer Verwendungszweck ist das Bleichen oder Desinfizieren (beispielsweise in Schwimmbädern). Die Verwendung in Schwimmbädern ist nicht unproblematisch, da die zu dosierenden Mengen ausreichen müssen, um das anwesende Ammoniak (bzw. die Amine) über die Stufe des Monochloramins hinaus zu chlorieren, da erst dann eine ausreichende Desinfektion gewährleistet ist. Natriumhypochlorit ist auch der wesentliche Wirkbestandteil von desinfizierenden und bleichenden Haushaltsreinigern wie DanKlorix und vielen anderen. Auch diverse Schimmelentferner enthalten diesen Wirkstoff. Weiterhin findet Natriumhypochlorit Anwendung in der Zahnmedizin. So wird es beispielsweise bei der Wurzelkanalbehandlung bakteriell infizierter Zähne eingesetzt, um diese zu desinfizieren. SicherheitshinweiseBeim Umgang mit Natriumhypochlorit ist höchste Vorsicht geboten! Es besteht Explosionsgefahr bei der Reaktion von Natriumhypochlorit mit zahlreichen Stoffen und Stoffgruppen, darunter Reduktionsmitteln, Aminen, Ameisensäure, Methanol, organischen Substanzen und einige weiteren. Greift beim einatmen die Schleimhäute stark an. Des Weiteren reagiert Natriumhypochlorit mit Säuren (z. B. Salzsäure, Salpetersäure) und Oxidationsmitteln (z. B. Wasserstoffperoxid, Permanganate) zum Teil sehr heftig unter Hitzeentwicklung und Freisetzung von Chlorgas und/oder nitrosen Gasen. Schon durch Erwärmung oder Sonnenlicht kann es zum Zerfall von Natriumhypochlorit kommen, bei dem unter anderem Chlor, Chlorwasserstoff, Chlordioxid und Sauerstoff freigesetzt werden. Dies ist auch bei der Lagerung des Stoffes zu berücksichtigen. Quellen
Kategorien: Ätzender Stoff | Umweltgefährlicher Stoff | Natriumverbindung | Hypochlorit |
||||||||||||||||||||||||||||||||||||||||||||||||
| Dieser Artikel basiert auf dem Artikel Natriumhypochlorit aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. | ||||||||||||||||||||||||||||||||||||||||||||||||