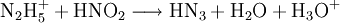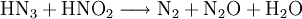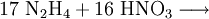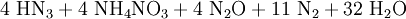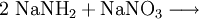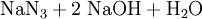Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Stickstoffwasserstoffsäure
Stickstoffwasserstoffsäure ist eine chemisch instabile, die Schleimhäute reizende Flüssigkeit. Sie ist äußerst explosiv. Das Azid-Ion N3− ist linear gebaut und isoelektronisch mit den Kohlenstoffdioxid-Molekül. Die Salze der Stickstoffwasserstoffsäure werden Azide genannt. Aufgrund der Instabilität der Säure werden Azide allerdings nicht über die Stickstoffwasserstoffsäure erzeugt, sondern über das Natriumazid. Die Stickstoffwasserstoffsäure wird durch die Einwirkung der stärkeren Schwefelsäure auf das Natriumazid gewonnen. Produkt-Highlight
Gewinnung und Darstellung
EigenschaftenStickstoffwasserstoffsäure ist eine farblose, leicht bewegliche Flüssigkeit. Sie ist hochexplosiv. Wasserfreie Stickstoffwasserstoffsäure explodiert beim Erwärmen und bei geringer Erschütterung. Auch konzentrierte Lösungen dürfen weder erhitzt noch plätschernd umgefüllt oder mit dem Gefäß hart aufgesetzt werden. Verdünnte wässrige Lösungen bis 20 % HN3 sind gefahrlos zu handhaben. Als Behältermaterial sind Polyethylen, Glas, Edelstahl, Aluminium und Titan geeignet. VerwendungNatriumazid wird als Konservierungsmittel für Milchuntersuchungsproben und in der chemischen Synthese zur Einführung von Azidgruppen (-N3) und zur Darstellung von Triazolen verwendet. Ein Gemisch aus Natriumazid, Kaliumperchlorat, Eisen(III)-oxid, Füllstoff und Binder dient als Treibladung für Airbags. Einige Salze der Stickstoffwasserstoffsäure, insbesondere Bleiazid und Silberazid, sind als Initialsprengstoffe brauchbar. Polyglycidylazid (GAP, (C3H5N3O)n) ist ein Polymerisat, das als energiereicher Binder in Feststoffraketen verwendet wird.
VerbindungenDie Salze der Stickstoffwasserstoffsäure sind in manchen Eigenschaften den Chloriden ähnlich. Silberazid und Bleiazid sind farblos, schwerlöslich und hochexplosiv. Natriumazid (NaN3) ist in Wasser leicht löslich (420 g/L), lässt sich unzersetzt schmelzen und zerfällt ab 300 °C in kontrollierbarer Reaktion in metallisches Natrium und Stickstoff. Kupferazid Cu(N3)2 ist extrem brisant und explodiert oft schon bei Berührung. ToxikologieStickstoffwasserstoffsäure ist sehr giftig, stark schleimhautreizend und hat einen unerträglichen durchdringenden Geruch. Beim Einatmen geringer Mengen entsteht zunächst ein Druckgefühl in der Nase. Die tödliche Dosis beträgt weniger als 5 mg pro kg Körpergewicht. Vergiftungssymptome sind Übelkeit, Kopfschmerz, Schwindel, Blutdruckabfall und Herzrasen. Quellen
Kategorien: Giftiger Stoff | Explosionsgefährlicher Stoff | Mineralsäure | Stickstoffverbindung | Azid | Pseudohalogen |
||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dieser Artikel basiert auf dem Artikel Stickstoffwasserstoffsäure aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. | ||||||||||||||||||||||||||||||||||||||||||||||||||||