Ein neuer Elektrolyt für umweltfreundlichere und sicherere Batterien
Neues Material verbessert die Leistung von Natrium-Festkörperbatterien - eine weniger gefährliche und haltbarere Alternative zu Lithium
Anzeigen
Die Zukunft der Batterietechnologie liegt im Natrium. Natrium ist nachhaltiger als Lithium - das derzeit die meisten unserer Geräte und Fahrzeuge antreibt - und kommt auf der Erdoberfläche reichlich vor. Das einzige Problem besteht darin, dass sich seine Ionen im flüssigen Elektrolyt herkömmlicher Batterien nur schwer bewegen lassen, wodurch es weniger effizient ist als Lithium. Die Lösung liegt daher in der Entwicklung eines festen Elektrolyten. Einem wissenschaftlichen Team der Universität Genf (UNIGE) ist es gelungen, diese Herausforderung zu meistern, indem es die Kristallstruktur eines Materials aus Kohlenstoff, Bor und Wasserstoff (Carbo-Hydridoborat) verändert hat. Die Forschungsgruppe definierte auch den idealen Druck, der auf die Batterie ausgeübt werden muss, damit sie effizient funktioniert. Die Ergebnisse sind in den Fachzeitschriften ACS Applied Materials & Interfaces und Advanced Materials Interfaces nachzulesen.

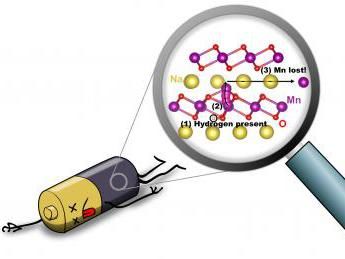
Der vom UNIGE-Team entwickelte feste Elektrolyt ermöglicht eine effiziente Bewegung der Ionen in den Natriumbatterien.
Xavier Ravinet / Olivier Gaumer – UNIGE
Lithium-Ionen-Batterien (oder "Li-Ion"-Batterien), die Anfang der 1990er Jahre auf den Markt kamen, treiben heute die meisten unserer elektronischen Geräte und Elektrofahrzeuge an. Sie haben jedoch zwei große Schwachstellen. Der in ihnen enthaltene flüssige Elektrolyt, der den Fluss positiver Ionen zwischen den beiden Elektroden der Batterie ermöglicht, ist hochentzündlich. Wenn er ausläuft, kann er heftig mit Sauerstoff reagieren, was eine große Gefahr für die Benutzer darstellt. Auch die Versorgung mit Lithium ist problematisch: Es ist ungleichmäßig über den Globus verteilt und steht ebenso wie Erdöl im Mittelpunkt wichtiger geopolitischer Fragen.
Eine Alternative ist die Natriumbatterie. Dieses chemische Element ist überall auf der Erde und im Meer reichlich vorhanden und billiger als Lithium. Außerdem ist es leichter zu recyceln. Seine Verwendung ist jedoch noch unterentwickelt. "Die Herstellung dieser Art von Batterien erfordert eine andere Technologie als die der Lithium-Batterien. Die Industrie zögert noch, sich auf diese weniger bekannte Technologie einzulassen", erklärt Fabrizio Murgia, Forscher im Kristallographielabor der UNIGE-Fakultät für Naturwissenschaften.
Das derzeit effizienteste Material
Da Natrium schwerer ist als Lithium, bewegen sich seine Ionen im flüssigen Elektrolyten auch weniger leicht. Die Lösung besteht darin, einen festen Elektrolyten zu entwickeln, der auch nicht entflammbar ist. Die bisher entwickelten Elektrolyte dieser Art, die aus Hydridoboraten (Bor und Wasserstoff) bestehen, konnten jedoch nicht die Leistung von Lithiumbatterien erreichen. Zwei kürzlich durchgeführte Studien des UNIGE-Kristallographielabors unter der Leitung von Professor Radovan Cerny konnten dieses Problem lösen.
Die erste, die in ACS Applied Materials & Interfaces veröffentlicht wurde, führte zur Entwicklung eines effizienten Materials: Natriumcarbo-hydridoborat (NaCB11H12). "Ursprünglich ist dieses Material, das in der Nuklearmedizin verwendet wird, nicht leitfähig", erklärt Radovan Cerny. "Durch eine Veränderung der Kristallstruktur, genauer gesagt der räumlichen Anordnung der Atome, ist es uns gelungen, es leitfähig zu machen, was es zum derzeit effizientesten Mittel für den Transport von Natriumionen macht." Um dieses Ergebnis zu erzielen, setzte das Forscherteam die Verbindung in einer Kugelmühle starken Stößen aus, die hohe Temperaturen erzeugten. Dies ist eine energieeffiziente Methode, die in der Zementindustrie weit verbreitet ist.
"Einfach" zu produzieren
Das zweite Forschungsprojekt, das in Advanced Materials Interfaces veröffentlicht wurde, bestand darin, dieses Material in eine Situation zu bringen. Damit eine Batterie funktioniert, muss der Elektrolyt, ob flüssig oder fest, in engem Kontakt mit der positiven und negativen Elektrode der Batterie stehen. Er muss also fest in der Batterie eingeschlossen sein. "Um dies zu erreichen, muss mit Hilfe von Schrauben oder Federn Druck ausgeübt werden. Wir haben nach der idealen 'Kraft' gesucht, die auf unseren Festelektrolyten ausgeübt werden kann", erklärt Matteo Brighi, ehemaliger Postdoktorand im Kristallographielabor. Es zeigte sich, dass diese etwa 400 Atmosphären betragen sollte, was dem Druck unter Wasser in 4 000 Metern Tiefe entspricht und mit einigen Schraubenumdrehungen sehr leicht erreicht werden kann.
Diese Entdeckungen ebnen den Weg für eine einfachere Produktion von Natriumbatterien, insbesondere für die Automobilindustrie. "Wegen des etwas höheren Gewichts dieser Batterien könnten sie vor allem für den Antrieb von Autos verwendet werden. Auch die Kosteneffizienz ihrer Herstellung muss noch bewertet werden, aber es ist jetzt wichtig, dass die Industrie erkennt, dass das von uns entdeckte Material wirklich interessant ist", schließt Fabrizio Murgia.
Hinweis: Dieser Artikel wurde mit einem Computersystem ohne menschlichen Eingriff übersetzt. LUMITOS bietet diese automatischen Übersetzungen an, um eine größere Bandbreite an aktuellen Nachrichten zu präsentieren. Da dieser Artikel mit automatischer Übersetzung übersetzt wurde, ist es möglich, dass er Fehler im Vokabular, in der Syntax oder in der Grammatik enthält. Den ursprünglichen Artikel in Englisch finden Sie hier.
Originalveröffentlichung
Weitere News aus dem Ressort Wissenschaft
Meistgelesene News
Weitere News von unseren anderen Portalen
Verwandte Inhalte finden Sie in den Themenwelten
Themenwelt Batterietechnik
Die Themenwelt Batterietechnik bündelt relevantes Wissen in einzigartiger Weise. Hier finden Sie alles über Anbieter und deren Produkte, Webinare, Whitepaper, Kataloge und Broschüren.

Themenwelt Batterietechnik
Die Themenwelt Batterietechnik bündelt relevantes Wissen in einzigartiger Weise. Hier finden Sie alles über Anbieter und deren Produkte, Webinare, Whitepaper, Kataloge und Broschüren.