Instabiles Molekül "klickt" mit synthetischer Strategie
Anzeigen
Die Elemente im Periodensystem der Elemente sind in einer Weise aufgelistet, die bestimmte Beziehungen hervorhebt. Es gibt Familien, Perioden (die horizontalen Zeilen) und Gruppen (die vertikalen Spalten). Die Elemente innerhalb jeder dieser Gruppierungen weisen einige Gemeinsamkeiten auf.
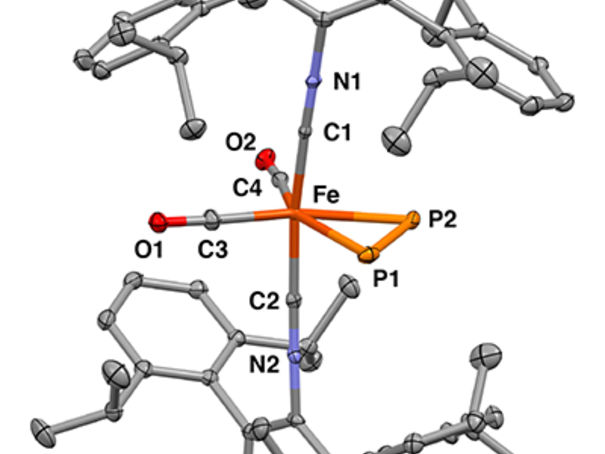
Röntgenkristallstruktur des mononuklearen Eisen-η2-Diphosphor-Komplexes
Figueroa Lab Group, UC San Diego / Curtis Moore, Ohio State University
Diagonale Beziehungen im Periodensystem bestehen zwischen zwei Elementen in diagonaler Position zueinander, die ähnliche chemische Eigenschaften aufweisen. Lithium und Magnesium, Bor und Silizium sowie Kohlenstoff und Phosphor sind Beispiele dafür.
Eine ikonische diagonale Beziehung besteht seit langem zwischen Kohlenstoff und Phosphor, insbesondere in Fällen, in denen Element-Element-Mehrfachbindungen vorhanden sind, wie z. B. bei Diphosphor (P2), bei dem zwei Phosphoratome durch eine schwache Dreifachbindung verbunden sind.
Diese diagonale Beziehung zwischen Phosphor und Kohlenstoff hat die Erwartung geweckt, dass das Diphosphormolekül die Eigenschaften des Kohlenwasserstoffs Acetylen (C2H2) nachahmen sollte. So reagieren sowohl Diphosphor als auch Acetylen mit anderen organischen Molekülen über ihre pi-Bindungen, eine Art von kovalenter Bindung, die in Molekülen mit Mehrfachbindungen zu finden ist.
Ein Koordinationskomplex besteht aus einem zentralen Atom oder Ion, das in der Regel metallisch ist und von gebundenen Molekülen oder Ionen, den so genannten Liganden oder Komplexbildnern, umgeben ist. Koordinationskomplexe sind für das Leben auf der Erde lebenswichtig und umfassen Hämoglobin und Chlorophyll. Auch in der Industrie werden sie in großem Umfang als Katalysatoren eingesetzt.
Obwohl die Koordinationschemie von Acetylen mit einzelnen Übergangsmetallen gut dokumentiert ist, waren Koordinationskomplexe, bei denen Diphosphor an ein einzelnes Metallzentrum gebunden ist, bisher nicht bekannt.
Kürzlich berichteten Forscher der University of California San Diego, der University of Rochester und der Ohio State University über die Bindung von Diphosphor an ein einzelnes Metallzentrum. Diese Arbeit erscheint in der Ausgabe vom 25. März in Science.
Diphosphor ist - anders als Acetylen - sehr instabil und reaktiv. In freier Form polymerisiert Diphosphor schnell oder reagiert mit vorhandenen Substratmolekülen. Mit anderen Worten: Diphosphor bleibt nicht lange Diphosphor - es liegt in seiner Natur, sich mit anderen Elementen und Molekülen zu verbinden. Das macht es schwierig, es zu untersuchen oder zu manipulieren.
Es gibt mehrere synthetische Verfahren zur Bildung mehrkerniger Diphosphorkomplexe. Die beliebteste Methode ist die Abspaltung des tetraedrischen P4-Moleküls, das allgemein als weißer Phosphor bekannt ist. Weißer Phosphor ist jedoch giftig und leicht entzündlich (er war ein Hauptbestandteil vieler Brandbomben, die im Zweiten Weltkrieg eingesetzt wurden).
"Die hier vorgestellte Arbeit bietet eine synthetische Strategie für den Zugang zu einkernigen Diphosphorkomplexen im Labor", erklärte Joshua Figueroa, Professor für Chemie und Biochemie an der UC San Diego, Hauptautor der Studie und Mitautor der Arbeit. "Wir gehen davon aus, dass dieser Koordinationsmodus die Entwicklung von selektiven Phosphor-Atom-Transferreaktionen auf organische Moleküle weiter ermöglichen wird".
Bei der Planung des Experiments verwendeten Figueroa und der Postdoktorand Shuai Wang von der UC San Diego Eisen als Metallion, weil es eine gute Koordinationsplattform bietet, die eine effiziente Bindung kleiner Moleküle ermöglicht. Indem sie Diphosphor an ein Eisenion banden, konnten sie die beiden Phosphoratome so zusammenfügen, dass die freie Freisetzung von Diphosphor umgangen wurde, was zu der begehrten Stabilität führte.
Wang, der Erstautor der Studie ist und die synthetischen Arbeiten durchführte, sagte: "In Anbetracht der extremen Empfindlichkeit des freien Diphosphormoleküls als flüchtige Spezies ist es bemerkenswert, wie stabil es wird, wenn es sich an das sterisch belastete einkernige Eisenzentrum koordiniert."
Die Forscher nutzten die Röntgenkristallographie, um die genaue 3D-Struktur der Moleküle zu bestimmen, und die Mossbauer-Spektroskopie, um Veränderungen in den Bindungswechselwirkungen zwischen dem Eisenion und dem Diphosphor zu beobachten. Dies war eine Schlüsseltechnik, denn damit konnten die Forscher zeigen, dass Diphosphor und ein Acetylenmolekül die Eigenschaften des Eisenzentrums auf ähnliche Weise beeinflussen.
Wenn Diphosphor in einer relativ stabilen und selektiv reaktiven Form vorliegt, können Wissenschaftler ihn in der so genannten "Klick"-Chemie an Substrate binden. Die Klick-Chemie beschreibt nicht eine einzige, spezifische Reaktion, sondern eine Art und Weise, Stoffe durch das Zusammenfügen kleiner modularer Einheiten zu erzeugen. Dies könnte neue Entdeckungsbereiche in der synthetischen Chemie für die Herstellung von pharmazeutischen Verbindungen eröffnen.
"Wir freuen uns über diese Arbeit, weil sie zeigt, wie wichtig es ist, grundlegende Konzepte, die man im ersten Jahr Chemie lernt, für neue Entdeckungen zu nutzen", sagte Figueroa.
Hinweis: Dieser Artikel wurde mit einem Computersystem ohne menschlichen Eingriff übersetzt. LUMITOS bietet diese automatischen Übersetzungen an, um eine größere Bandbreite an aktuellen Nachrichten zu präsentieren. Da dieser Artikel mit automatischer Übersetzung übersetzt wurde, ist es möglich, dass er Fehler im Vokabular, in der Syntax oder in der Grammatik enthält. Den ursprünglichen Artikel in Englisch finden Sie hier.