Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Elektron
In den bisher möglichen Experimenten zeigen Elektronen keine innere Struktur und können insofern als punktförmig angenommen werden. Die experimentelle Obergrenze für die Größe des Elektrons liegt derzeit bei etwa 10−19 m. In Atomen und in Ionen bilden Elektronen die Elektronenhülle. Jedes der gebundenen Elektronen lässt sich dabei eindeutig durch vier Quantenzahlen (n, l, m und s) beschreiben (siehe auch Pauli-Prinzip). Die freie Beweglichkeit einiger der Elektronen in Metallen ist die Ursache für die elektrische Leitfähigkeit von metallischen Leitern. Der experimentelle Nachweis von Elektronen gelang erstmals im Jahre 1897 durch den Briten Joseph John Thomson. Beim Betazerfall eines Atomkerns wird (unabhängig von der Atomhülle) ein Elektron erzeugt und emittiert. EigenschaftenEin Elektron ist ein „Quantenobjekt“, das heißt, bei ihm liegt die durch die Heisenbergsche Unschärferelation beschriebene Orts- und Impulsunschärfe im messbaren Bereich, so dass, ähnlich wie beim Licht, sowohl Wellen- als auch Teilcheneigenschaften beobachtet werden können. In einem Atom kann das Elektron als stehende Materiewelle betrachtet werden. Das Elektron ist das leichteste elektrisch geladene Elementarteilchen. Wegen Ladungserhaltung und Energieerhaltung müssen Elektronen daher stabil sein. In der Tat gibt es bisher keinerlei experimentellen Hinweis auf einen Elektronenzerfall; die Lebensdauer des Elektrons muss nach den experimentellen Daten größer als 1024 Jahre sein. Elektronen gehören zu den Leptonen und haben, wie alle Leptonen, einen Spin von ½. Als Teilchen mit halbzahligem Spin gehören sie zur Klasse der Fermionen, unterliegen also insbesondere dem Pauli-Prinzip. Ihre Antiteilchen sind die Positronen, Symbol e+, mit denen sie bis auf ihre elektrische Ladung in allen Eigenschaften übereinstimmen. Elektronen, die sich in polaren Lösungsmitteln wie Wasser oder Alkoholen von ihren Atomen gelöst haben, werden als solvatisierte Elektronen bezeichnet. Bei Lösung von Alkalimetallen in Ammoniak sind sie für die starke Blaufärbung verantwortlich. Einige der Grundeigenschaften des Elektrons, die in der Tabelle rechts aufgelistet sind, werden durch das magnetische Moment des Elektronenspins miteinander verknüpft:
In der Kathodenstrahlröhre bzw. Braunschen Röhre treten Elektronen aus einer beheizten Glühkathode aus und werden im Vakuum durch ein elektrisches Feld in Feldrichtung (in Richtung der positiven Anode) beschleunigt. Durch Magnetfelder werden die Elektronen senkrecht zur Feldrichtung und senkrecht zur augenblicklichen Flugrichtung abgelenkt (Lorentzkraft). Diese Eigenschaften der Elektronen haben erst die Entwicklung des Fernsehers und des Computermonitors sowie ihre Nutzung in technologischen Anwendungen (Elektronenkanone) ermöglicht. Die Masse eines ruhenden Elektrons ist konstant. Bei bewegten Elektronen (und ein Elektron ist unter normalen Bedingungen immer in Bewegung) muss die Massenzunahme nach der Relativitätstheorie berücksichtigt werden. An Elektronen kann diese Massenzunahme gut beobachtet werden, da sie sich aufgrund ihrer Ladung und geringen Masse leicht auf hohe Geschwindigkeiten beschleunigen lassen. Die Masse kann dann durch Ablenkung in einem Magnetfeld bestimmt werden. Die Zunahme der Masse eines Elektrons wurde zuerst von Walter Kaufmann 1901 nachgewiesen. In einem Festkörper erfährt das Elektron Wechselwirkungen mit dem Kristallgitter. Sein Verhalten lässt sich dann beschreiben, indem statt der Elektronenmasse die abweichende effektive Masse eingesetzt wird, die auch noch abhängig von der Bewegungsrichtung des Elektrons ist. Von der Ausdehnung des Elektrons zu unterscheiden ist sein Wirkungsquerschnitt für Wechselwirkungsprozesse. Bei der Streuung von Röntgenstrahlen an Elektronen erhält man einen Wirkungsquerschnitt, der einem effektiven Elektronenradius von etwa 3 · 10−15 m entspräche. Dieselbe Größenordnung ergäbe sich bei einer klassischen (nicht quantentheoretischen) Beschreibung des Elektrons unter den Annahmen:
Der totale Streuquerschnitt von Photonen an Elektronen beträgt im Grenzfall kleiner Photonenenergien 8/3 π re2, wobei re der klassische Elektronenradius ist (siehe Thomson-Streuung und Compton-Streuung). Siehe auch: Stern-Gerlach-Versuch |
||||||||||||||||||||||||||
| Dieser Artikel basiert auf dem Artikel Elektron aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. | ||||||||||||||||||||||||||





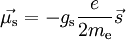 .
Dabei ist
.
Dabei ist 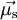 das magnetische Moment des Elektronenspins,
das magnetische Moment des Elektronenspins, 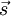 der
der 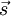 , der das Verhältnis aus magnetischem Moment zum Spin beschreibt, wird als
, der das Verhältnis aus magnetischem Moment zum Spin beschreibt, wird als 

