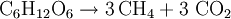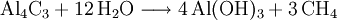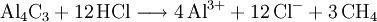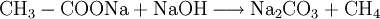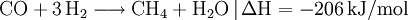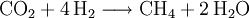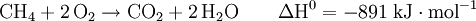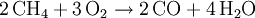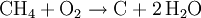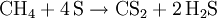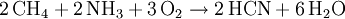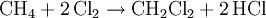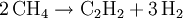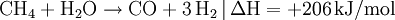Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Methan
Methan (auch Sumpfgas und Methylwasserstoff genannt) ist ein farbloses und geruchloses Gas. Das Wort stammt wohl aus dem griechischen "Μεθάνιον αέριον" (Methanion Aerion) und zeigt, daß auch die Griechen schon von dem entzündlichen Gas wußten. So gab es in Kleinasien Orte, an denen sich Methangas-Quellen entzündeten. Ein Vulkangebiet, in dem solche Gase vorkamen, bekam nach diesem Gas auch den Namen "Methana". Es ist das einfachste Alkan und der einfachste Kohlenwasserstoff überhaupt, die Summenformel lautet CH4, die C–H-Bindungen weisen in die Ecken eines Tetraeders. Methan ist der Hauptbestandteil von Erdgas und Biogas und ein wichtiger Bestandteil von Holzgas. Nach Kohlenstoffdioxid ist es das bedeutendste von Menschen freigesetzte Treibhausgas, wobei es 20 bis 30 mal wirkungsvoller ist, allerdings in kleineren Mengen in der Atmosphäre vorkommt. Dort reagiert es mit Sauerstoff zu Kohlenstoffdioxid und Wasser. Dieser Prozess ist allerdings langsam, die Halbwertszeit wird auf 14 Jahre geschätzt. Methan wird als Heizgas verwendet und dient als Ausgangspunkt für viele andere organische Verbindungen. Methan wird bei biologischen und geologischen Prozessen ständig neu gebildet und freigesetzt. Weiteres empfehlenswertes Fachwissen
Historische InformationenMethan war bereits den Alchemisten im Mittelalter als Fäulnisgas unter der Bezeichnung Sumpfluft bekannt. Methan wurde 1667 von Thomas Shirley entdeckt. 1772 entdeckte Joseph Priestley, dass Methan bei Fäulnisprozessen entsteht. 1856 stellte Marcellin Berthelot Methan zum ersten Mal aus Kohlenstoffdisulfid und Schwefelwasserstoff her. Eigenschaften
Physikalische EigenschaftenMethan ist ein farb- und geruchloses Gas, dessen Dichte kleiner ist als die von Luft, es steigt also in die höheren Schichten der Atmosphäre auf. Es ist brennbar und verbrennt mit bläulicher, nicht rußender Flamme, unterhält die Verbrennung aber nicht. Methan schmilzt bei −182,6 °C und siedet bei −161,7 °C. Aufgrund der unpolaren Eigenschaften ist es in Wasser kaum löslich, in Ethanol und Diethylether löst es sich jedoch gut. Schmelzwärme und Verdampfungswärme sind mit 1,1 kJ/mol und 8,17 kJ/mol für ein Gas relativ hoch, im Vergleich zu Metallen sind dies aber sehr geringe Werte. Der Heizwert Hi liegt bei 35,89 MJ·m−3. Die Standardentropie beträgt 188 J/mol·K, die Wärmekapazität 35,69 J/mol·K. Bei 90,67 K und 0,117 bar weist Methan einen Tripelpunkt auf, bei 190,56 K und 45,96 bar einen kritischen Punkt. Die UN-Nummern von verdichtetem und tiefgekühlten Methan sind 1971 bzw. 1972. Chemische EigenschaftenMethan kann explosionsartig mit Sauerstoff, Luft und Chlor reagieren. Bei der Chlorierung entstehen Methylchlorid, Dichlormethan, Chloroform und Tetrachlormethan. Bei der Oxidation dagegen wird das Molekül komplett auseinandergerissen. Aus der Reaktion eines Methanmoleküls mit zwei Sauerstoffmolekülen entstehen zwei Wasser- und ein Kohlenstoffdioxidmolekül. Vom Methan leiten sich Methylverbindungen wie z. B. Methanol und die Methylhalogenide sowie die längerkettigen Alkane ab. Vorkommen und Entstehung
Methan kommt vielfältig vor und wird auf der Erde ständig neu gebildet, auch auf vielen anderen Planeten gibt es Methanvorkommen. Auf Meeresböden gibt es festes Methanhydrat. Die weltweiten Methanhydratvorkommen werden auf 500–3000 Gt C geschätzt.[2][3] Zum Vergleich: Die nachgewiesenen Kohlereserven betragen ca. 900 Gt C.[4] Für deren Bergung gibt es aber noch kein Mittel. Eine Gewinnung des Methanhydrats könnte zur Lösung des Energieproblemes beitragen; ein besonderes Problem dabei besteht zum Beispiel darin, dass bei der Bergung viel Methan in die Atmosphäre gelangen würde und dort als starkes Treibhausgas zu einer weiteren Erwärmung und damit weiterer Freisetzung von Methan beitragen würde. Außerdem ist die Förderung von Methanhydrat (austretendes Methan am Meeresgrund wird durch den hohen Druck und die tiefe Temperatur zu Methanhydrat komprimiert) nicht ungefährlich. Erste Förderungsversuche sind bereits im Gange. Die Folgen eines Raubbaus sind weitgehend ungeklärt – Forscher befürchten das Abrutschen der Kontinentalabhänge, welche zu großen Teilen aus Methaneis (welches durch die Förderung instabil werden könne) bestehen. Methan ist Hauptbestandteil des Erdgases (85-98%). Auch das in Steinkohlelagern eingeschlossene Grubengas enthält hauptsächlich Methan.
Weltweit werden schätzungsweise jährlich 500 Millionen Tonnen Methan emittiert, etwa 70 % davon sind auf den Menschen zurückzuführen. Auch durch landwirtschaftlichen Anbau und Tierhaltung wird Methan emittiert, 39 % dieser Emissionen gehen auf die Rinderhaltung zurück, 17 % auf den Nassreisanbau. In Deutschland wurden 1994 etwa 833.000 Tonnen Methan emittiert. Die Konzentration in der Atmosphäre hat sich von 1750 zu 2000 von 0,8 auf 1,75 ppm erhöht. Beim Faulen organischer Stoffe unter Luftabschluss in Sümpfen oder am Grund stark verschmutzter Gewässer bildet sich Sumpfgas, ein Gemisch aus Methan und Kohlenstoffdioxid. Biogas besteht überwiegend aus Methan (etwa 60 %) und Kohlenstoffdioxid (etwa 35 %), daneben enthält es noch Wasserstoff, Stickstoff und Schwefelwasserstoff. Bei Stoffwechselvorgängen der Methanbildner entsteht Methan nach folgender Reaktionsgleichung:
Methan entsteht ebenfalls in tieferen Erdschichten bei hohen Temperaturen und Drücken. Diese Quellen setzen Methan meist bei vulkanischen Aktivitäten frei. In der Atmosphäre des Mars wurde Methan nachgewiesen, allerdings nur etwa 10,5 ppb. Da es sich normalerweise nicht in der Atmosphäre halten kann und es keine Hinweise auf Meteoriten als Quelle gibt, muss es auf dem Mars neu gebildet worden sein, was ein Indiz für Leben sein kann. Allerdings könnte das Methan auch vulkanischen Ursprungs sein, es wurden aber bis jetzt keine Hinweise dafür gefunden. Auch in den Atmosphären von Titan, Jupiter, Saturn, Uranus, Neptun und Pluto gibt es Methanvorkommen. Im Weltall ist Methan also in größeren Mengen auf Planeten, Kometen sowie Monden vorhanden. HerstellungFür die Herstellung aus Aluminiumcarbid gibt es zwei Methoden, sie werden allerdings meist nur im Labor eingesetzt. Die Synthese aus Kohlenstoffmonoxid hat eine besondere Wichtigkeit, da das giftige Kohlenstoffmonoxid, das eigentlich unerwünscht/unbrauchbar ist, sinnvoll genutzt werden kann, lediglich die Quelle des Wasserstoffs stellt bei dieser Synthese ein Problem dar.
Heute wird auch viel Methan als Brennstoff in Biogasanlagen hergestellt. Auch durch Holzvergasung kann Methan gewonnen werden. Umgang, Gefahren und SicherheitMit einem Luftvolumenanteil zwischen 5 und 15 Prozent bildet es explosive Gemische. Durch unbemerktes Ausströmen von Erdgas kommt es immer wieder zu folgeschweren Gasexplosionen. Auch die gefürchteten Grubengasexplosionen in Kohlebergwerken (Schlagwetter) sind auf Methan-Luft-Gemische zurückzuführen. Methan ist hochentzündlich, der Flammpunkt liegt bei −188 °C, die Zündtemperatur bei 600 °C. Methanbehälter sollen an gut belüfteten Orten aufbewahrt werden, es sollte von Zündquellen ferngehalten werden und es sollten Maßnahmen gegen elektrostatische Aufladung getroffen werden. Methan wird unter hohen Drücken und meist bei tiefen Temperaturen (um die Dichte zu erhöhen) aufbewahrt, in Gasflaschen bei 150 bar, in Tankerschiffen bei etwa −160 °C. Methan wird bei tiefen Temperaturen flüssig gelagert, weil die Dichte dadurch enorm erhöht werden kann. Aus diesem Grund kann es beim Austritt dieses gekühlten Methans leicht zu Erfrierungen kommen. Methan ist ungiftig, die Aufnahme von Methan kann allerdings zu erhöhten Atem- (Hyperventilation) und Herzfrequenzen führen, es kann kurzzeitig zu niedrigem Blutdruck, Taubheit in den Extremitäten, Schläfrigkeit, mentaler Verwirrung und Gedächtnisverlust, alles hervorgerufen durch Sauerstoffmangel, führen. Methan führt aber nicht zu bleibenden Schäden. Wenn die Symptome auftreten, sollte das betroffene Areal verlassen und tief eingeatmet werden, falls daraufhin die Symptome nicht verschwinden, sollte die betroffene Person in ein Krankenhaus gebracht werden. VerwendungHeute wird die bakterielle Zersetzung organischer Verbindungen zunehmend wirtschaftlich genutzt, indem man aus Mist und Gülle, Klärschlamm oder organischem Müll Biogas gewinnt. Bereits früher wurde Methan durch Pyrolyse von Holz gewonnen (Holzvergasung). Das Biogas und die weiteren Methangasgemische werden zur Wärmegewinnung und Energiegewinnung genutzt. Holzgas diente im Zweiten Weltkrieg zum Betrieb von Automobilen. Methan ist ein wichtiges Ausgangsprodukt für technische Synthesen von Wasserstoff, Methanol, Ethin, Blausäure, Schwefelkohlenstoff und Methylhalogeniden. Künftig könnte Methan als Treibstoff für die Rückkehr bemannter Mars-Missionen eingesetzt werden. Die Mars Society hat ein Konzept ausgearbeitet, um aus dem in der Mars Atmosphäre vorkommenden Kohlenstoffdioxid (CO2) nach dem Sabatier-Prozess Methan zu gewinnen.
ReaktionenReaktionen mit SauerstoffMit Sauerstoff geht Methan unterschiedliche Reaktionen ein, je nachdem wie viel Sauerstoff für die Reaktion zur Verfügung steht. Nur bei genügend großem Sauerstoffangebot ist eine vollständige Verbrennung des Methans mit optimaler Energieausbeute möglich.[5] Bei ungenügender Sauerstoffzufuhr hingegen entstehen unerwünschte Nebenprodukte wie Kohlenstoffmonoxid (CO) und Kohlenstoff (Ruß). Ferner ist in diesem Fall die Nutzenergie geringer. Weitere ReaktionenMethan geht außer mit Sauerstoff noch vielfältige weitere Reaktionen ein. Viele davon sind sehr wichtig für die chemische Industrie, da die Entstehungsprodukte von großer technischer Bedeutung sind.
Biologie, Geologie und KlimatologieMethan ist ein wichtiges Treibhausgas. Das Erwärmungspotential von Methan ist 25 mal höher als das von Kohlenstoffdioxid. Die zunehmende Haltung von Rindern und der häufige Nassreisanbau führen zu einer Verstärkung des Treibhauseffektes. Die Methanbildner sind für die ständige Neubildung von Methan hauptverantwortlich. Ein Hausrind stößt täglich etwa 150–250 l Methan aus, weil im Rindermagen Methanbildner bei der Zersetzung von Zellulose helfen. Neue Erkenntnisse zeigen, dass Pflanzen ständig Methan produzieren und so schon immer zum Methan-Gehalt der Atmosphäre beitragen.[6] Methan war neben Ammoniak und Wasserdampf ein wichtiger Bestandteil der Uratmosphäre. Hierbei soll es nach Stanley Miller eine wichtige Rolle bei der Entstehung der Erdatmosphäre gespielt haben. In einem Versuch setzte er diese Gase eine Woche lang elektrischen Entladungen aus, wobei zahlreiche organische Verbindungen, unter anderem Aminosäuren, entstanden. In einer sauerstoffhaltigen Atmosphäre wird Methan langsam, insbesondere durch Hydroxyl-Radikale, oxidiert. Ein einmal in die Atmosphäre gelangtes Methan-Molekül hat dort eine durchschnittliche Verweilzeit von zwölf Jahren. Methan auf TitanAuf dem Saturnmond Titan herrscht bei −180 °C und ca. 1,6 Bar Atmosphärendruck fast der Tripelpunkt des Methans. Methan kann deshalb auf diesem Mond in allen drei Aggregatzuständen auftreten. Es gibt Wolken aus Methan, aus denen Methan regnet, das dann durch Flüsse in Methanseen fließt, dort wieder verdunstet und so einen geschlossenen Methankreislauf bildet (analog zum Wasserkreislauf auf der Erde). Quellen
LiteraturBücher
Siehe auch
Kategorien: Feuergefährlicher Stoff | Alkan | Gas |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dieser Artikel basiert auf dem Artikel Methan aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||