Neuer Weg zu chemisch recycelbaren Kunststoffen
"Hier geht es darum, wirklich coole Chemie zu verstehen und zu versuchen, damit etwas Gutes zu tun"
Anzeigen
Da die Belastung des Planeten durch Gummi- und Plastikmüll ungebremst ansteigt, blicken Wissenschaftler zunehmend auf das Versprechen eines geschlossenen Recyclingkreislaufs, um Abfall zu reduzieren. Ein Team von Forschern am Fachbereich Chemie in Princeton gibt die Entdeckung eines neuen Polybutadien-Moleküls bekannt - aus einem Material, das seit über einem Jahrhundert bekannt ist und zur Herstellung gängiger Produkte wie Reifen und Schuhe verwendet wird -, das dieses Ziel eines Tages durch Depolymerisation vorantreiben könnte.
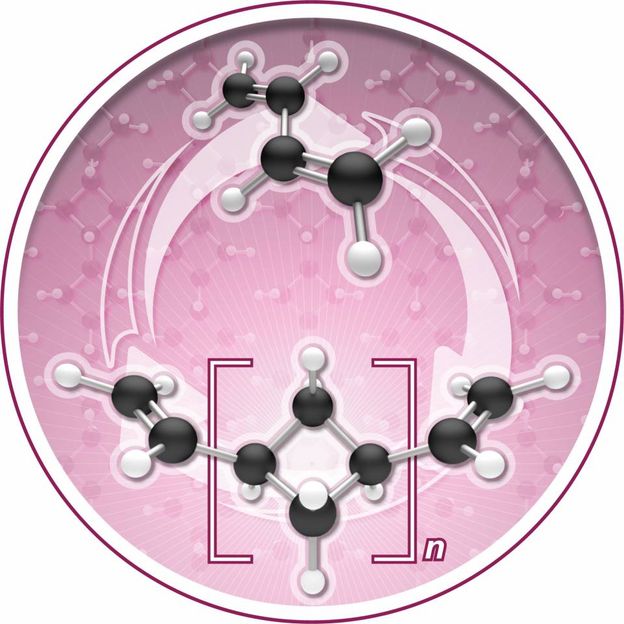
Iron-catalyzed [2+2] oligomerization of butadiene produces (1,n'-divinyl)oligocyclobutane, a new polymer that can be chemically recycled.
Figure by Jonathan Darmon of the Princeton University Department of Chemistry
Das Chirik-Labor berichtet in Nature Chemistry, dass sich das Molekül mit dem Namen (1,n'-Divinyl)oligocyclobutan während der Polymerisation in einer sich wiederholenden Abfolge von Quadraten verkettet, einer bisher nicht realisierten Mikrostruktur, die es ermöglicht, den Prozess unter bestimmten Bedingungen rückwärts laufen zu lassen, also zu depolymerisieren.
Mit anderen Worten, das Butadien kann "aufgezippt" werden, um ein neues Polymer herzustellen; dieses Polymer kann dann wieder zu einem ursprünglichen Monomer entpackt werden, um wieder verwendet zu werden.
Die Forschung befindet sich noch in einem frühen Stadium und die Leistungseigenschaften des Materials müssen noch gründlich erforscht werden. Aber das Chirik-Labor hat einen konzeptionellen Präzedenzfall für eine chemische Umwandlung geschaffen, die im Allgemeinen für bestimmte Gebrauchsmaterialien nicht für praktikabel gehalten wird.
In der Vergangenheit wurde die Depolymerisation mit teuren Nischen- oder Spezialpolymeren und nur nach einer Vielzahl von Schritten durchgeführt, aber nie aus einem so häufig vorkommenden Rohstoff wie dem, der zur Herstellung von Polybutadien verwendet wird, einem der sieben wichtigsten petrochemischen Grundstoffe der Welt. Butadien ist eine häufig vorkommende organische Verbindung und ein wichtiges Nebenprodukt der Entwicklung fossiler Brennstoffe. Es wird zur Herstellung von synthetischem Gummi und Kunststoffprodukten verwendet.
"Eine ganz gewöhnliche Chemikalie zu nehmen, die seit vielen Jahrzehnten erforscht und polymerisiert wird, und daraus ein grundlegend neues Material zu machen - ganz zu schweigen davon, dass dieses Material interessante angeborene Eigenschaften hat - das ist nicht nur unerwartet, sondern wirklich ein großer Schritt nach vorn. Man würde nicht unbedingt erwarten, dass an diesem Baum noch Früchte hängen", sagt Alex E. Carpenter, Chemiker bei ExxonMobil Chemical, der an der Forschung beteiligt war.
"Der Schwerpunkt dieser Zusammenarbeit lag für uns auf der Entwicklung neuer Materialien, die der Gesellschaft zugute kommen, indem wir uns auf einige neue Moleküle konzentrieren, die [der Princeton-Chemiker] Paul Chirk entdeckt hat und die ziemlich transformativ sind", so Carpenter weiter.
"Die Menschheit ist gut darin, Butadien herzustellen. Es ist sehr schön, wenn man andere nützliche Anwendungen für dieses Molekül finden kann, denn wir haben reichlich davon."
Katalyse mit Eisen
Das Chirik-Labor erforscht nachhaltige Chemie, indem es die Verwendung von Eisen - einem weiteren reichlich vorhandenen natürlichen Material - als Katalysator zur Synthese neuer Moleküle untersucht. In dieser speziellen Forschung klickt der Eisenkatalysator die Butadienmonomere zusammen, um Oligocyclobutan herzustellen. Aber er tut dies in einem höchst ungewöhnlichen quadratischen Strukturmotiv. Normalerweise erfolgt die Verkettung mit einer S-förmigen Struktur, die oft als spaghettiähnlich beschrieben wird.
Um die Depolymerisation zu bewirken, wird das Oligocyclobutan in Gegenwart des Eisenkatalysators einem Vakuum ausgesetzt, das den Prozess umkehrt und das Monomer zurückgewinnt. Die Arbeit des Chirik-Labors mit dem Titel "Iron Catalyzed Synthesis and Chemical Recycling of Telechelic, 1,3-Enchained Oligocyclobutanes" (Eisenkatalysierte Synthese und chemisches Recycling von telechelen, 1,3-verketteten Oligocyclobutanen) bezeichnet dies als ein seltenes Beispiel für chemisches Recycling in einem geschlossenen Kreislauf.
Megan Mohadjer Beromi, Postdoktorandin im Labor von Chirik, hat zusammen mit Chemikern des Polymer-Forschungszentrums von ExxonMobil die faszinierenden Eigenschaften des Materials beschrieben. Zum Beispiel ist es telechelisch, das heißt, die Kette ist an beiden Enden funktionalisiert. Diese Eigenschaft könnte es ermöglichen, es als eigenständigen Baustein zu verwenden, der als Brücke zwischen anderen Molekülen in einer Polymerkette dient. Darüber hinaus ist es thermisch stabil, d.h. es kann auf über 250 Grad Celsius erhitzt werden, ohne dass es sich schnell zersetzt.
Schließlich weist es eine hohe Kristallinität auf, selbst bei einem niedrigen Molekulargewicht von 1.000 Gramm pro Mol (g/mol). Dies könnte darauf hindeuten, dass wünschenswerte physikalische Eigenschaften - wie Kristallinität und Materialfestigkeit - bei niedrigeren Gewichten erreicht werden können als allgemein angenommen. Das in der durchschnittlichen Plastik-Einkaufstüte verwendete Polyethylen hat zum Beispiel ein Molekulargewicht von 500.000 g/mol.
"Eines der Dinge, die wir in der Arbeit demonstrieren, ist, dass man aus diesem Monomer wirklich zähe Materialien herstellen kann", sagt Chirik, Edwards S. Sanford Professor für Chemie in Princeton. "Die Energie zwischen Polymer und Monomer kann eng beieinander liegen, und man kann hin und her gehen, aber das bedeutet nicht, dass das Polymer schwach sein muss. Das Polymer selbst ist stark.
"Die Leute neigen zu der Annahme, dass ein chemisch recycelbares Polymer von Natur aus schwach oder nicht haltbar sein muss. Wir haben etwas geschaffen, das sehr, sehr widerstandsfähig ist, aber auch chemisch recycelbar ist. Wir können daraus reines Monomer zurückgewinnen. Und das hat mich überrascht. Das ist nicht optimiert. Aber es ist da. Die Chemie ist sauber.
"Ich glaube wirklich, dass diese Arbeit eine der wichtigsten ist, die je aus meinem Labor kam", sagt Chirik.
Weg mit dem Ethylen
Das Projekt reicht ein paar Jahre zurück bis 2017, als C. Rose Kennedy, damals Postdoc im Labor von Chirik, eine zähflüssige Flüssigkeit bemerkte, die sich während einer Reaktion am Boden eines Kolbens ansammelte. Kennedy sagte, sie habe erwartet, dass sich etwas Flüchtiges bilden würde, und das Ergebnis weckte ihre Neugierde. Als sie die Reaktion genauer untersuchte, entdeckte sie eine Verteilung von Oligomeren - oder nichtflüchtigen Produkten mit niedrigem Molekulargewicht - die darauf hinwiesen, dass eine Polymerisation stattgefunden hatte.
"Mit dem, was wir bereits über den Mechanismus wussten, war es sofort klar, wie es möglich sein würde, sie auf eine andere oder kontinuierliche Weise zusammenzuklicken. Wir erkannten sofort, dass dies etwas potenziell äußerst Wertvolles sein könnte", so Kennedy, der heute Assistenzprofessor für Chemie an der University of Rochester ist.
Zu diesem frühen Zeitpunkt verkettete Kennedy Butadien und Ethylen. Es war Mohadjer Beromi, der später vermutete, dass es möglich wäre, das Ethylen ganz zu entfernen und nur reines Butadien bei erhöhten Temperaturen zu verwenden. Mohadjer Beromi "gab" das vierkettige Butadien an den Eisenkatalysator, und das ergab das neue Polymer aus Quadraten.
"Wir wussten, dass das Motiv die Neigung hat, chemisch recycelt zu werden", sagte Mohadjer Beromi. "Aber ich denke, eine der neuen und wirklich interessanten Eigenschaften des Eisenkatalysators ist, dass er [2+2]-Cycloadditionen zwischen zwei Dienen durchführen kann, und das ist es, was diese Reaktion im Wesentlichen ist: Es ist eine Cycloaddition, bei der man zwei Olefine miteinander verknüpft, um ein quadratisches Molekül immer und immer wieder herzustellen.
"Das ist das Coolste, woran ich je in meinem Leben gearbeitet habe."
Um Oligocyclobutan weiter zu charakterisieren und seine Leistungseigenschaften zu verstehen, musste das Molekül skaliert und in einer größeren Einrichtung mit Expertise in neuen Materialien untersucht werden.
"Woher wissen Sie, was Sie gemacht haben?" fragte Chirik. "Wir haben einige der normalen Werkzeuge benutzt, die wir hier in Frick haben. Aber was wirklich wichtig ist, sind die physikalischen Eigenschaften dieses Materials, und wie die Kette letztendlich aussieht."
Dafür reiste Chirik letztes Jahr nach Baytown, Texas, um die Ergebnisse des Labors bei ExxonMobil vorzustellen, das sich entschloss, die Arbeit zu unterstützen. Ein integriertes Team von Wissenschaftlern aus Baytown war an der rechnerischen Modellierung, an Röntgenstreuungsarbeiten zur Validierung der Struktur und an zusätzlichen Charakterisierungsstudien beteiligt.
Recycling 101
Die chemische Industrie verwendet eine kleine Anzahl von Bausteinen, um die meisten handelsüblichen Kunststoffe und Gummi herzustellen. Drei solcher Beispiele sind Ethylen, Propylen und Butadien. Eine große Herausforderung beim Recycling dieser Materialien besteht darin, dass sie oft mit anderen Additiven kombiniert und verstärkt werden müssen, um Kunststoffe und Kautschuke herzustellen: Additive sorgen für die gewünschten Leistungseigenschaften - die Härte einer Zahnpastakappe zum Beispiel oder die Leichtigkeit einer Einkaufstüte. Diese "Zutaten" müssen im Recyclingprozess alle wieder getrennt werden.
Aber die chemischen Schritte, die mit dieser Trennung verbunden sind, und der Energieaufwand, der dafür erforderlich ist, machen das Recycling unerschwinglich, insbesondere für Einwegkunststoffe. Plastik ist billig, leicht und praktisch, aber es wurde nicht mit Blick auf die Entsorgung entwickelt. Das, so Chirik, ist das Hauptproblem, das sich immer mehr verschlimmert.
Als mögliche Alternative zeigt die Forschung von Chirik, dass das Butadien-Polymer energetisch fast gleichwertig mit dem Monomer ist, was es zu einem Kandidaten für das chemische Recycling in einem geschlossenen Kreislauf macht.
Chemiker vergleichen den Prozess der Herstellung eines Produkts aus einem Rohmaterial mit dem Hinaufrollen eines Felsblocks auf einen Hügel, wobei die Spitze des Hügels den Übergangszustand darstellt. Von diesem Zustand aus rollt man den Felsbrocken auf der anderen Seite hinunter und erhält am Ende ein Produkt. Aber bei den meisten Kunststoffen sind die Energie und die Kosten, um den Felsbrocken rückwärts den Berg hinaufzurollen, um das Rohmonomer zu gewinnen, schwindelerregend und daher unrealistisch. Also landen die meisten Plastiktüten, Gummiprodukte und Stoßstangen auf der Mülldeponie.
"Das Interessante an dieser Reaktion, bei der eine Einheit Butadien an die nächste angehängt wird, ist, dass das 'Ziel' nur geringfügig energieärmer ist als das Ausgangsmaterial", sagt Kennedy. "Das macht es möglich, in die andere Richtung zurückzugehen."
In der nächsten Phase der Forschung, so Chirik, wird sich sein Labor auf die Verkettung konzentrieren, die die Chemiker bisher im Durchschnitt nur bis zu 17 Einheiten erreicht haben. Bei dieser Kettenlänge wird das Material kristallin und so unlöslich, dass es aus dem Reaktionsgemisch herausfällt.
"Wir müssen lernen, was wir damit machen können", sagt Chirik. "Wir sind durch seine eigene Stärke begrenzt. Ich würde gerne ein höheres Molekulargewicht sehen."
Dennoch sind die Forscher begeistert von den Aussichten für Oligocyclobutan, und viele Untersuchungen sind in dieser fortlaufenden Zusammenarbeit in Richtung chemisch recycelbarer Materialien geplant.
"Mit den Materialien, die wir heute haben, können wir nicht alle Probleme lösen, die wir zu lösen versuchen", sagt Carpenter. "Der Glaube ist, dass, wenn man gute Wissenschaft betreibt und in peer-reviewed Journalen publiziert und mit Weltklasse-Wissenschaftlern wie Paul zusammenarbeitet, dann wird das unser Unternehmen in die Lage versetzen, wichtige Probleme auf konstruktive Art und Weise zu lösen."
"Hier geht es darum, wirklich coole Chemie zu verstehen", fügte er hinzu, "und zu versuchen, damit etwas Gutes zu tun."
Hinweis: Dieser Artikel wurde mit einem Computersystem ohne menschlichen Eingriff übersetzt. LUMITOS bietet diese automatischen Übersetzungen an, um eine größere Bandbreite an aktuellen Nachrichten zu präsentieren. Da dieser Artikel mit automatischer Übersetzung übersetzt wurde, ist es möglich, dass er Fehler im Vokabular, in der Syntax oder in der Grammatik enthält. Den ursprünglichen Artikel in Englisch finden Sie hier.