Verbesserte Pharmazeutika dank Fluor
Ein neues Werkzeug für den Wasserstoff-Fluor-Tausch macht Medikamente wirksamer
Anzeigen
Die Entwicklung und Verbesserung von Pharmazeutika spielt eine zentrale Rolle im fortlaufenden Kampf gegen Krankheiten. Die Organische Chemie ermöglicht diesen Fortschritt, indem sie Methoden bereitstellt, mit denen man chemische Strukturen verändern kann. Ein Forscherteam um Chemiker Nuno Maulide von der Universität Wien und Harald Sitte von der Medizinischen Universität Wien hat nun ein neues Werkzeug entdeckt. Die Wissenschafter fanden eine Möglichkeit, mit der Wasserstoff in wichtigen Arzneimitteln mühelos durch Fluor ersetzt werden kann – dasselbe Fluor, das auch in Zahnpasta verwendet wird. Diese neue Entdeckung erlaubt die Feinabstimmung von bereits bekannten (sowie auch potentiell neuen) Pharmazeutika.
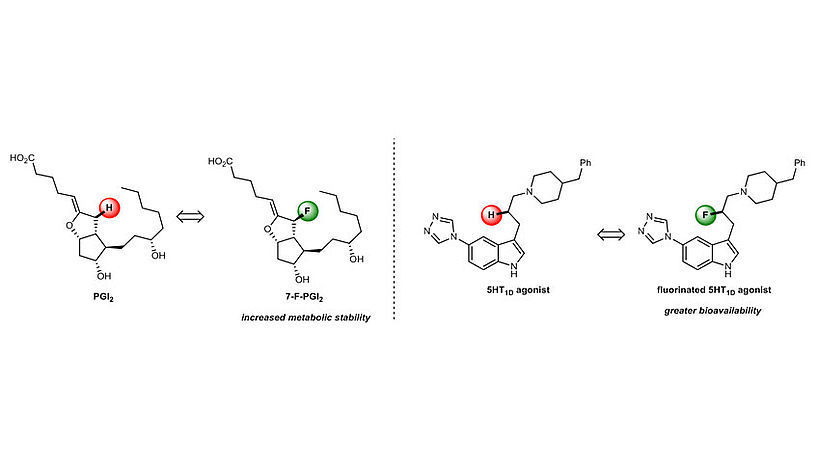
Links: Austausch eines Wasserstoffatoms (rot) durch Fluor (grün) führt zu einer stark erhöhten metabolischen Stabilität. Rechts: Die gleiche kleine Veränderung führt zu einer größeren Bioverfügbarkeit.
© Universität Wien/Maulide Group
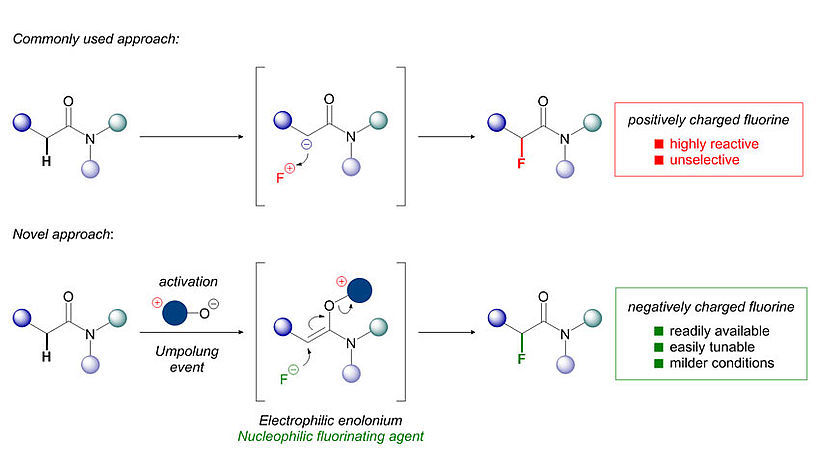
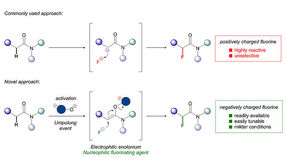
Der weit verbreitete Ansatz zur Fluorierung verwendet unerwünschte Reagenzien und ist oft unselektiv (oben). Im Gegensatz dazu erlaubt dieAktivierung eines Amids, gefolgt von sogenannter Umpolung (Polaritätsinversion) die Verwendung von erwünschtem F–, das eine Reihe an Vorteilen gegenüber seinem Gegenstück, dem F+, bietet.
© Universität Wien/Maulide Group
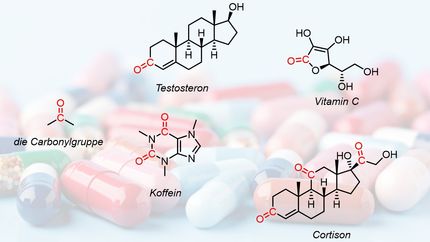
Die große Mehrheit der Pharmazeutika, die zur Behandlung menschlicher Erkrankungen angewandt werden, ist organischer Natur. Ihre aktive Komponente ist ein Molekül (oder eine Kombination aus mehreren Molekülen), welches aus Kohlenstoff- und Wasserstoffatomen aufgebaut ist. "Unsere Körper sind nichts anderes als eine Ansammlung von Milliarden Kohlenstoffverbindungen, oder in anderen Worten, organischen Molekülen", erklärt Nuno Maulide, Österreichs Wissenschafter des Jahres 2018, von der Universität Wien. Durch diese Ähnlichkeit sind organische Pharmazeutika ideal, um mit dem menschlichen Körper zu interagieren.
Der Entwurf eines pharmakologischen Moleküls passend zu einer spezifischen Interaktion mit einem Rezeptor wird oft mit dem Schlüssel-Schloss Prinzip erklärt. "Der Rezeptor (oft ein Enzym) hat eine einzigartige Struktur (Schloss) und benötigt daher auch eine einzigartige Struktur (Schlüssel), mit der er interagieren kann. Der Schlüssel zu einer vorteilhaften Bioaktivität ist die strukturelle Unversehrtheit der pharmazeutischen Verbindung um die exakte Passform zu gewährleisten", erklärt Harald Sitte von der Medizinischen Universität Wien und Koautor der Studie.
Allerdings werden Pharmazeutika, die in den Körper gelangen, von denselben Enzymen abgebaut, die auch Essensbestandteile verarbeiten. "Diese Art von Aufräummaschinerie ist für unseren Körper zwar essentiell um ihn zu schützen, unglücklicherweise ist sie oft nicht spezifisch und Pharmazeutika werden metabolisiert, sobald sie in den Körper gelangen", stellt Christopher Teskey, Ko-Erstautor der Studie, fest. Dadurch können Medikamente ihre vorteilhaften Eigenschaften verlieren. "Ein Großteil dieses Abbaus erfolgt an der Bindungsstelle zwischen Kohlenstoff- (C) und Wasserstoffatomen (H). C–H Bindungen sind von Natur aus ziemlich schwach, was bedeutet, dass sie leicht oxidiert werden können", erklärt Co-Erstautorin Pauline Adler.
Einen vielversprechenden Ansatz, um dieses Problem zu lösen, haben Chemiker vor einigen Jahren entdeckt: Den Tausch von besonders schwachen C–H Bindungen mit viel stärkeren C–F Bindungen. Obwohl sich Wasserstoff und Fluor in manchen Aspekten stark unterscheiden, sind deren Größen vergleichbar und man kann davon ausgehen, dass der Austausch nur einen minimalen Effekt auf die Struktur des Medikaments hat, wie Maulide erklärt: "Durch dessen unterschiedliche elektronische Eigenschaften kann ein strategisch platziertes Fluoratom zusätzliche Interaktionen mit dem Ziel erzeugen und dadurch den erwünschten Effekt verstärken." Zudem könne das Einführen von Fluor in ein Medikament dessen Eigenschaften so verändern, dass es leichter vom Körper aufgenommen werden könne, ergänzt Daniel Kaiser, Koautor der Studie.
Die Einführung von Fluor kann eine Vielzahl von vorteilhaften Effekten auf Pharmazeutika haben, jedoch ist die Platzierung auf organische Moleküle oft nicht einfach. "Die meisten Chemiker versuchten Fluor einzuführen, indem sie negativ polarisierte organische Moleküle mit einem F+-Reagenz reagieren ließen. Wir haben das Gegenteil gemacht: Wir wechselten die Polarität des organischen Moleküls, sodass wir dasselbe Fluorid verwenden konnten, das auch in Zahnpasta verwendet wird". Der neu entwickelte Ansatz verwendet günstiges Ausgangsmaterial und ist einfach zu handhaben", freut sich Maulide. "Eine Methode um Wasserstoff unter einfachen Bedingungen mit Fluor zu ersetzen, ist nur der Anfang. Wir können uns vorstellen, dies mit einer Reihe anderer Pharmazeutika zu machen und die Eigenschaften der neu erzeugten Analoga zu erforschen."
Originalveröffentlichung
Weitere News aus dem Ressort Wissenschaft
Meistgelesene News
Weitere News von unseren anderen Portalen
Verwandte Inhalte finden Sie in den Themenwelten
Themenwelt Synthese
Die chemische Synthese steht im Zentrum der modernen Chemie und ermöglicht die gezielte Herstellung von Molekülen mit spezifischen Eigenschaften. Durch das Zusammenführen von Ausgangsstoffen in definierten Reaktionsbedingungen können Chemiker eine breite Palette von Verbindungen erstellen, von einfachen Molekülen bis hin zu komplexen Wirkstoffen.

Themenwelt Synthese
Die chemische Synthese steht im Zentrum der modernen Chemie und ermöglicht die gezielte Herstellung von Molekülen mit spezifischen Eigenschaften. Durch das Zusammenführen von Ausgangsstoffen in definierten Reaktionsbedingungen können Chemiker eine breite Palette von Verbindungen erstellen, von einfachen Molekülen bis hin zu komplexen Wirkstoffen.