Wissenschaftler suchen nach Atompaaren, die die Aktivität eines Katalysators verstärken
Die chaotische Umgebung einer chemischen Reaktion kann die Form eines katalytischen Nanopartikels tatsächlich so verändern, dass er aktiver wird
Anzeigen
Der Ersatz der teuren Metalle, die die Abgase in Katalysatoren abbauen, durch billigere, effektivere Materialien hat für die Wissenschaftler höchste Priorität, sowohl aus wirtschaftlichen als auch aus ökologischen Gründen. Katalysatoren werden benötigt, um chemische Reaktionen durchzuführen, die sonst nicht stattfinden würden, wie z.B. die Umwandlung umweltschädlicher Gase aus Autoabgasen in saubere Verbindungen, die in die Umwelt freigesetzt werden können. Um sie zu verbessern, brauchen Forscher ein tieferes Verständnis der genauen Funktionsweise von Katalysatoren.

In einer Studie am SLAC und in Stanford wurde ermittelt, welche Atompaare in einem Katalysator-Nanopartikel bei einer Reaktion, die ein schädliches Abgas in Katalysatoren zersetzt, am aktivsten sind. Die aktivsten Partikel enthielten den größten Anteil einer bestimmten Atomkonfiguration - einer, bei der zwei Atome, die jeweils von sieben benachbarten Atomen umgeben sind, Paare bilden, um die Reaktionsschritte durchzuführen.
Greg Stewart/SLAC National Accelerator Laboratory
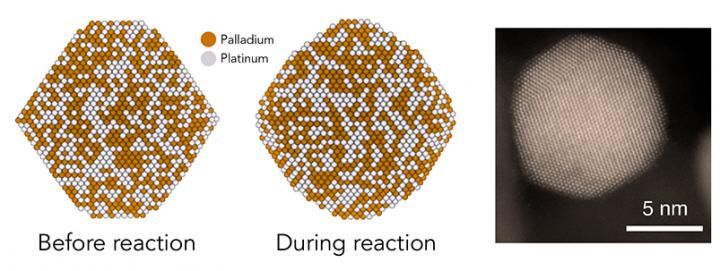
In einer Studie am SLAC und in Stanford sagten Theoretiker voraus, dass Katalysator-Nanopartikel aus Palladium und Platin (links) bei bestimmten chemischen Reaktionen (Mitte) runder werden und stufenförmige Merkmale mit Atompaaren erzeugen, die besonders aktive katalytische Stellen sind. Experimente und elektronenmikroskopische Aufnahmen, wie die rechts, bestätigten, dass dies der Fall ist, was ein neues Verständnis der Funktionsweise von Katalysatoren ermöglicht.
Greg Stewart/SLAC National Accelerator Laboratory

Nun hat ein Team der Universität Stanford und des SLAC National Accelerator Laboratory des Energieministeriums genau ermittelt, welche Atompaare in einem Nanopartikel aus Palladium und Platin - eine Kombination, die häufig in Konvertern verwendet wird - bei der Zersetzung dieser Gase am aktivsten sind.
Sie beantworteten auch eine Frage, die die Katalysatorforscher vor ein Rätsel gestellt hat: Warum funktionieren größere Katalysatorpartikel manchmal besser als kleinere, wenn man das Gegenteil erwarten würde? Die Antwort hat mit der Art und Weise zu tun, wie die Partikel im Verlauf der Reaktionen ihre Form verändern und mehr dieser hochaktiven Stellen erzeugen.
Die Ergebnisse sind ein wichtiger Schritt hin zur Entwicklung von Katalysatoren für eine bessere Leistung sowohl bei industriellen Prozessen als auch bei der Emissionskontrolle, sagte Matteo Cargnello, ein Assistenzprofessor für chemische Verfahrenstechnik in Stanford, der das Forschungsteam leitete.
"Das aufregendste Ergebnis dieser Arbeit war die Feststellung, wo die katalytische Reaktion stattfindet - an welchen atomaren Orten kann man diese Chemie durchführen, die ein umweltschädliches Gas in unschädliches Wasser und Kohlendioxid verwandelt, was unglaublich wichtig und unglaublich schwierig ist", sagte Cargnello. "Jetzt, da wir wissen, wo sich die aktiven Stellen befinden, können wir Katalysatoren entwickeln, die besser funktionieren und weniger teure Inhaltsstoffe verwenden.
In einem Autokatalysator sind Nanopartikel aus Edelmetallen wie Palladium und Platin auf einer Keramikoberfläche angebracht. Beim Vorbeiströmen der Emissionsgase verklammern sich die Atome auf der Oberfläche der Nanopartikel an vorbeifliegenden Gasmolekülen und regen diese an, mit Sauerstoff zu Wasser, Kohlendioxid und anderen weniger schädlichen Chemikalien zu reagieren. Ein einziges Partikel katalysiert Milliarden von Reaktionen, bevor es sich erschöpft.
Die heutigen Katalysatoren seien so konstruiert, dass sie am besten bei hohen Temperaturen funktionieren, sagte Cargnello, weshalb die meisten schädlichen Abgasemissionen von Fahrzeugen stammen, die gerade erst anfangen, sich aufzuwärmen. Da immer mehr Motoren für den Betrieb bei niedrigeren Temperaturen konstruiert werden, ist es dringend notwendig, neue Katalysatoren zu finden, die bei diesen Temperaturen besser funktionieren, sowie in Schiffen und Lastwagen, die wahrscheinlich nicht in absehbarer Zeit auf elektrischen Betrieb umgestellt werden.
Aber was macht einen Katalysator aktiver als einen anderen? Die Antwort war schwer zu finden.
In dieser Studie betrachtete das Forschungsteam Katalysator-Nanopartikel aus Platin und Palladium aus zwei Perspektiven - Theorie und Experiment -, um zu sehen, ob sie spezifische atomare Strukturen auf ihrer Oberfläche identifizieren können, die zu einer höheren Aktivität beitragen.
Rundere Partikel mit gezackten Kanten
Was die Theorie betrifft, so schufen der SLAC-Mitarbeiter Frank Abild-Pedersen und seine Forschungsgruppe am SUNCAT Center for Interface Science and Catalysis einen neuen Ansatz zur Modellierung, wie die Exposition gegenüber Gasen und Dampf während chemischer Reaktionen die Form und atomare Struktur eines katalytischen Nanopartikels beeinflusst. Dies sei rechnerisch sehr schwierig, sagte Abild-Pedersen, und frühere Studien hätten angenommen, dass Partikel im Vakuum existierten und sich nie verändert hätten.
Seine Gruppe schuf neue und einfachere Wege, um Partikel in einer komplexeren, realistischeren Umgebung zu modellieren. Berechnungen der Postdoktoranden Tej Choksi und Verena Streibel ergaben, dass die achtseitigen Nanopartikel mit fortschreitender Reaktion runder werden und ihre flachen, facettenartigen Oberflächen zu einer Reihe von gezackten kleinen Schritten werden.
Durch die Herstellung und das Testen von Nanopartikeln unterschiedlicher Grösse, die jeweils ein unterschiedliches Verhältnis von gezackten Kanten zu flachen Oberflächen aufweisen, hoffte das Team herauszufinden, welche Strukturkonfiguration und sogar welche Atome am meisten zur katalytischen Aktivität der Partikel beitragen.
Ein wenig Hilfe durch Wasser
Angel Yang, ein Doktorand in der Gruppe von Cargnello, stellte Nanopartikel von genau kontrollierter Größe her, die jeweils eine gleichmäßig verteilte Mischung aus Palladium- und Platinatomen enthielten. Dazu musste sie eine neue Methode entwickeln, um die grösseren Partikel herzustellen, indem sie sie um die kleineren herum implantierte. Yang verwendete Röntgenstrahlen von SLACs Stanford Synchrotronstrahlungsquelle in Stanford, um die Zusammensetzung der Nanopartikel zu bestätigen, die sie mit Hilfe von SLACs Simon Bare und seinem Team hergestellt hatte.
Dann führte Yang Experimente durch, bei denen Nanopartikel unterschiedlicher Größe verwendet wurden, um eine Reaktion zu katalysieren, die Propen, einen der am häufigsten im Abgas enthaltenen Kohlenwasserstoffe, in Kohlendioxid und Wasser verwandelt.
"Wasser spielte hier eine besonders interessante und nützliche Rolle", sagte sie. "Normalerweise vergiftet es Katalysatoren oder deaktiviert sie. Aber hier machte die Exposition gegenüber Wasser die Partikel runder und öffnete aktivere Stellen.
Die Ergebnisse bestätigten, dass grössere Partikel aktiver waren und dass sie während der Reaktionen runder und zackiger wurden, wie die rechnergestützten Studien vorhersagten. Die aktivsten Teilchen enthielten den größten Anteil einer bestimmten Atomkonfiguration - einer, bei der zwei Atome, die jeweils von sieben benachbarten Atomen umgeben sind, Paare bilden, um die Reaktionsschritte durchzuführen. Es waren diese "7-7 Paare", die es großen Teilchen ermöglichten, bessere Leistungen zu erbringen als kleineren.
In Zukunft, so Yang, hofft sie herauszufinden, wie man Nanopartikel mit viel billigeren Materialien sät, um ihre Kosten zu senken und den Einsatz seltener Edelmetalle zu reduzieren.
Interesse der Industrie
Die Forschung wurde von der BASF über die California Research Alliance finanziert, die die Forschung zwischen BASF-Wissenschaftlern und sieben Universitäten an der Westküste, darunter Stanford, koordiniert.
"Dieses Paper befasst sich mit grundlegenden Fragen über aktive Standorte, wobei Theorie und experimentelle Perspektiven auf eine wirklich schöne Art und Weise zusammenkommen, um die experimentellen Phänomene zu erklären. Das wurde noch nie zuvor gemacht, und deshalb ist es ziemlich bedeutsam", sagte Yuejin Li, ein leitender Hauptwissenschaftler der BASF, der an der Studie teilnahm.
"Letztendlich", sagte er, "wollen wir ein theoretisches Modell haben, das vorhersagen kann, welches Metall oder welche Kombination von Metallen eine noch bessere Aktivität haben wird als unser derzeitiger Stand der Technik".
Hinweis: Dieser Artikel wurde mit einem Computersystem ohne menschlichen Eingriff übersetzt. LUMITOS bietet diese automatischen Übersetzungen an, um eine größere Bandbreite an aktuellen Nachrichten zu präsentieren. Da dieser Artikel mit automatischer Übersetzung übersetzt wurde, ist es möglich, dass er Fehler im Vokabular, in der Syntax oder in der Grammatik enthält. Den ursprünglichen Artikel in Englisch finden Sie hier.