Enzym-System für die Wasserstoff-Wirtschaft
Platinfreier Biokatalysator für Brennstoffzellen und Wasser-Elektrolyse
Anzeigen
Einen Traum der Energiewirtschaft könnte ein Enzym wahr werden lassen: Effizient kann es sowohl aus Strom Wasserstoff erzeugen, als auch Wasserstoff in Strom umwandeln. Zu seinem Schutz ist das Enzym in ein Polymer eingebettet. Ein internationales Forschungsteam mit maßgeblicher Beteiligung von Wissenschaftlern der Technischen Universität München (TUM) hat das System jetzt im Wissenschaftsjournal Nature Catalysis vorgestellt.
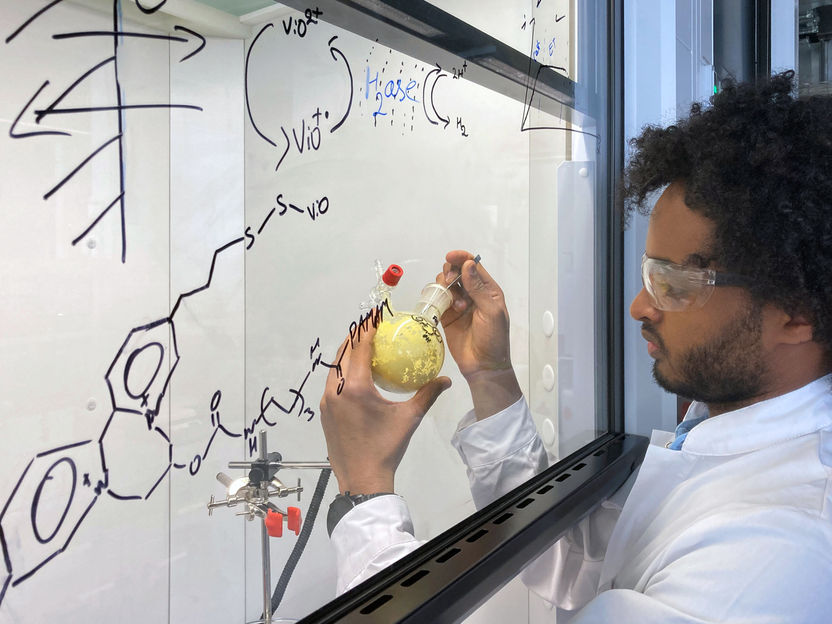
Dawit T. Filmon, Mitarbeiter von Prof. Nicolas Plumere, Professur für Elektrobiotechnologie am TUM Campus Straubing für Biotechnologie und Nachhaltigkeit, hält einen Ausgangsstoff für die Seitenketten des schützenden Polymers in seinen Händen.
Jan Winter / TUM
Sowohl Brennstoffzellen, die Wasserstoff in Strom umwandeln, als auch Elektrolyseure, die durch Wasserspaltung mithilfe von Strom Wasserstoff herstellen können, brauchen das seltene und damit teure Edelmetall Platin als Katalysator. Die Natur hat eine andere Lösung: Enzyme, sogenannte Hydrogenasen. Sie katalysieren die Umwandlung von Wasserstoff sehr schnell und nahezu ohne Energieverlust.
Allerdings galten diese Biokatalysatoren bisher als ungeeignet für den industriellen Einsatz, da sie hoch empfindlich gegen Sauerstoff sind. Einem Forschungsteam der TU München, der Ruhr-Universität Bochum, des CNRS Marseille und des Max-Planck-Instituts für Chemische Energiekonversion in Mülheim an der Ruhr ist es nun gelungen, die empfindlichen Enzyme so in ein schützendes Polymer einzubauen, dass sie auch für die technische Wasserstoffumwandlung eingesetzt werden können
Haltbarkeit und Aktivität im Widerstreit
„Bettet man die empfindlichen Hydrogenasen in geeignete Polymere ein, so arbeiten sie auch in Gegenwart von Sauerstoff mehrere Wochen“, sagt Nicolas Plumeré, Professor für Elektrobiotechnologie am TUM Campus Straubing für Biotechnologie und Nachhaltigkeit. „Ohne diesen Schutz verlieren sie ihre Aktivität innerhalb von Minuten.“
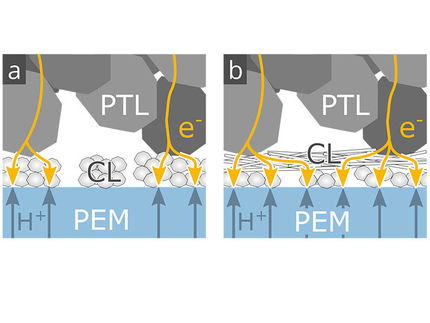
Das Einbetten in sogenannte Redox-Polymere, Kunststoffe, deren Seitengruppen Elektronen übertragen können, hatte jedoch bisher einen entscheidenden Nachteil: Sie setzten dem Fluss von Elektronen einen hohen Widerstand entgegen. Um ihn zu überwinden, musste man Energie investieren, die in Form von Wärme verloren ging. Die Fähigkeit, Wasserstoff zu erzeugen, büßten die eingebetteten Hydrogenasen dabei ganz ein.
Feinabstimmung des Potenzials
Durch geschickte Wahl der Polymer-Seitengruppen gelang es dem Forschungsteam nun, das Redoxpotenzial des Polymers so einzustellen, dass sie nur noch eine geringe Überspannung brauchten, um den Widerstand zu überwinden.
Bei genaueren Untersuchungen stellten sie fest, dass sich das Potenzial der Seitengruppen durch den Einbau in die Polymermatrix leicht zu positiven Werten hin verschoben hatte. In einem weiteren Anlauf setzten sie daher eine Seitengruppe mit einem entsprechend negativen Potenzial ein. Dieser Trick brachte den Durchbruch: Die Hydrogenase konnte nun die Reaktion ohne Energieverlust wieder in beiden Richtungen katalysieren.
Biokatalysator für die Wasserstoff-Umwandlung
Mit diesem System baute das Forschungsteam eine Brennstoffzelle auf. Sauerstoff wird in dieser durch das Enzym Bilirubin-Oxidase aus dem Bakterium Myrothecium verrucaria reduziert, während die im Polymerfilm eingebettete Hydrogenase aus dem Bakterium Desulfovibrio desulfuricans den Wasserstoff oxidiert und dabei Strom erzeugt.
Mit einer Leerlaufspannung von 1,16 V, dem höchsten jemals für ein System dieser Art gemessenen Wert, erreichte die Zelle einen Wert nahe des thermodynamischen Maximums. Gleichzeitig erreichte die Zelle mit drei Milliampere pro Quadratzentimeter eine für biologische Zellen sehr hohe Stromdichte.
Auch für die umgekehrte Reaktion, die Wasserstoffproduktion durch Aufnahme von Elektronen, ist das System einsetzbar: Seine Effizienz bei der Energieumwandlung liegt auch bei Stromdichten von über vier Milliampere pro Quadratzentimeter nahe 100 Prozent.
Blaupause für neue Biokatalysatoren
„Die Verringerung des Energieverlusts hat zwei entscheidende Vorteile“, sagt Nicolas Plumeré. „Das System wird dadurch nicht nur wesentlich effizienter. Bei hohen Leistungen wäre die in einem Brennstoffzellen-Stack entstehende Wärme für die biologischen Systeme ein Problem.“
Die weitere Forschung des Teams zielt nun drauf ab, die Stabilität der Hydrogenasen bei höheren Stromdichten zu verbessern, um Systemen mit Katalysatoren auf Platin-Basis Konkurrenz machen zu können.
Darüber hinaus können die Erkenntnisse auch auf andere hochaktive aber empfindliche Katalysatoren für Energieumwandlung und Elektrosynthese übertragen werden. Unmittelbare Ziele sind hier vor allem Kohlendioxid-reduzierende Enzyme, die mithilfe vom Strom flüssige Brennstoffe oder Zwischenprodukten aus Kohlendioxid herstellen können.