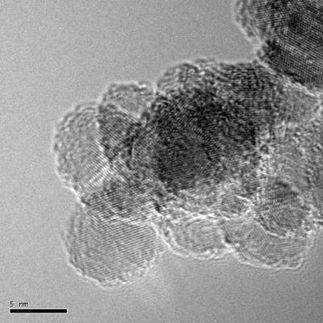
Nanodiamanten als Photokatalysatoren mit Sonnenlicht aktivierbar
Diese preiswerten Materialien könnten ein Schlüssel sein, um künftig mit Sonnenlicht CO₂ zu wertvollen Kohlenwasserstoffen weiter zu verarbeiten
Anzeigen
Nanodiamant-Materialien besitzen Potenzial als preisgünstige Photokatalysatoren. Doch bisher benötigten solche Kohlenstoff-Nanopartikel energiereiches UV-Licht, um aktiv zu werden. Das DIACAT-Konsortium hat daher Variationen von Nanodiamant-Materialien hergestellt und analysiert. Die Arbeit zeigt: Wenn die Oberfläche der Nanopartikel mit ausreichend Wasserstoff-Atomen besetzt ist, reicht auch die schwächere Energie von Licht im sichtbaren Bereich für die Anregung aus. Photokatalysatoren auf Basis von Nanodiamanten könnten in Zukunft mit Sonnenlicht CO2 oder N2 in Kohlenwasserstoffe oder Ammoniak umwandeln.
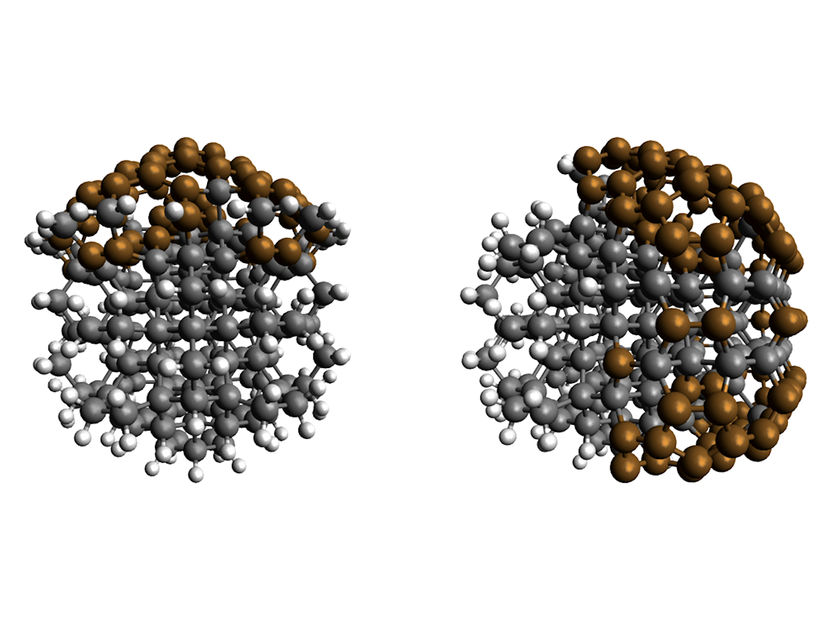
Die Illustration zeigt zwei Varianten von Nano-Diamant-Materialien mit unterschiedlichen Oberflächen: C230H106 links, C286H68 rechts. Sp3-C-Atome (Diamant) schwarz, sp3x C-Atome (Fulleren-artig) braun, H-Atome: Hellgrau. Bei teilweiser Belegung der Fläche mit Wasserstoff können Nanodiamanten schnell genug Licht im sichtbaren Bereich absorbieren und Elektronen in Lösung gehen.
T. Kirschbaum / HZB
Um chemische Reaktionen in einem wässrigen Medium katalytisch zu beschleunigen, kommt es darauf an, zunächst Elektronen aus einem Katalysator herauszulösen. Das kann mit Licht gelingen. Seit einigen Jahren stehen daher so genannte Nanodiamant-Materialien im Fokus der Forschung: Es sind preiswerte Nanopartikel aus Kohlenstoff, deren Oberflächen im Vergleich zum Volumen sehr groß sind. Bei reinen Kohlenstoff-Nanodiamant-Materialien wird jedoch (wie beim reinen Diamant) energiereiches UV-Licht für die Anregung benötigt. Weil sie so extrem winzig sind, können sich an den Oberflächen unter Umständen jedoch molekulare Zustände etablieren, die auch sichtbares Licht absorbieren.
Auf die Oberflächen kommt es an
Ein Team am HZB hat nun im Rahmen des DIACAT-Projekts unterschiedliche Varianten von Nanodiamant-Materialien während der Anregung mit Licht untersucht und die Prozesse dabei mit extrem hoher Zeitauflösung analysiert. Nanodiamantmaterialien mit unterschiedlicher Oberflächenterminierung stellte das Team um Dr. Jean-Charles Arnault, CEA, Frankreich, und die Gruppe um Prof. Anke Krueger, Universität Stuttgart, her. Dabei unterschieden sich die Nanopartikel durch ihre Oberflächen, die mal mehr, mal weniger zusätzliche Wasserstoffatome enthielten.
Wasserstoff hilft
„Der Wasserstoff an den Oberflächen erleichtert die Emission von Elektronen erheblich“, erklärt Dr. Tristan Petit, Nanodiamant-Experte am HZB. „Dabei ist eine bestimmte Kombination aus Wasserstoff sowie Fulleren-artigen Teilchen an den Oberflächen der Nanopartikel ideal“, sagt er.
UV-Licht funktioniert immer
„Wir haben die wässrigen Nanodiamantdispersionen mit verschiedenen Oberflächenabschlüssen wie Wasserstoff, -OH oder -COOH untersucht und mit verschiedenen Wellenlängen angeregt“, sagt Dr. Christoph Merschjann. Mit Hilfe von ultraschnellen Laserpulsen konnten sie genau vermessen, wie sich das Absorptionsprofil bei verschiedenen Anregungswellenlängen im UV-Bereich bei 225 nm und mit blauem Licht im sichtbaren Bereich bei 400 nm verhält.
Was passiert kurz nach der Anregung?
„Wir wollten herausfinden, was in den entscheidenden Pikosekunden nach Anregung mit Licht passiert, denn das ist die Zeit, in der ein Elektron die Oberfläche verlässt und ins Wasser geht“, sagt Merschjann. Das Theorieteam um Dr. Annika Bande steuerte Modellierungen mit Dichtefunktionaltheorie bei, um die Spektren zu interpretieren. Die Messdaten zeigten, wie erwartet, dass UV-Licht in allen Proben Elektronen in Lösung bringt, aber bei jenen Proben, die Fulleren-artigen Kohlenstoff an ihren Oberflächen hatten, gelang dies auch mit sichtbarem Licht.
Blaues Licht kann ausreichen
„In dieser Arbeit zeigen wir - nach unserem besten Wissen zum ersten Mal - dass die Emission von gelösten Elektronen aus Nanodiamanten in Wasser mit sichtbarem Licht möglich ist!“, fasst Petit die Ergebnisse zusammen. Damit ist ein entscheidender Schritt geschafft, um Nanodiamant-Materialien als Photokatalysatoren zu erschließen. Diese preiswerten und metallfreien Materialien könnten ein Schlüssel sein, um künftig mit Sonnenlicht CO2 zu wertvollen Kohlenwasserstoffen weiter zu verarbeiten oder auch N2 zu Ammoniak zu machen.