Neue Messmethode für die Anziehungskraft von Wasserstoffbrückenbindungen
Anzeigen
Mithilfe aufwändiger Computersimulationen haben Chemiker der Universität Paderborn eine neue Methode zur experimentellen Bestimmung der Bindungsstärke von Wasserstoffbrücken entwickelt.
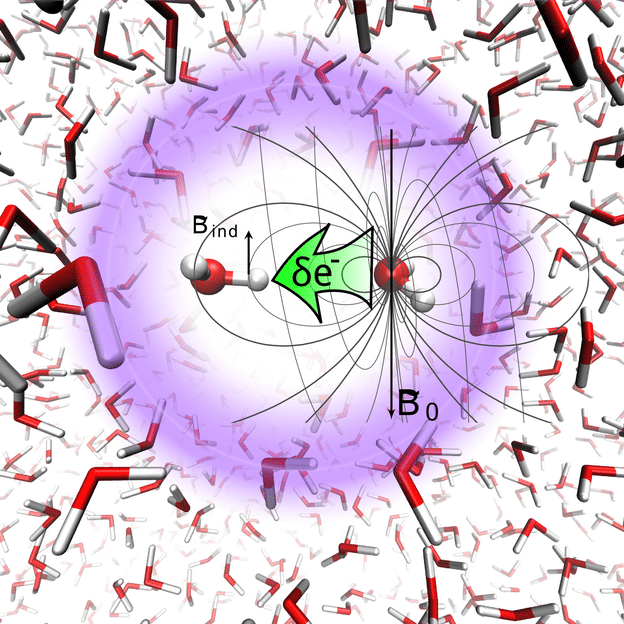
Positiv geladene Wasserstoffatome reagieren mit der negativen Ladung eines Sauerstoffatoms in einem benachbarten Wassermolekül. Die Anziehung kann jetzt erstmalig experimentell bestimmt werden.
Universität Paderborn
Wasserstoffbrücken sind für die speziellen Eigenschaften vieler für Lebewesen wichtiger Biomoleküle wie DNA, Proteine und Kohlenhydrate von enormer Bedeutung. War bisher nur eine grobe Klassifikation möglich, haben Chemiker der Universität Paderborn bei Computersimulationen jetzt eine Gleichung entdeckt, mit der die Stärke dieser Bindungen mithilfe von spektroskopischen Messungen (NMR) genau bestimmt werden kann.
Wasserstoffbrückenbindungen entstehen in der anziehenden Wechselwirkung von stark positiv polarisierten Wasserstoffatomen und freien Elektronenpaaren benachbarter Moleküle. Sie kommen vor allem in gasförmigen und flüssigen Stoffen, am stärksten in Wasser, vor und sind auch für Struktur und Funktion vieler Biomoleküle verantwortlich: So hängt etwa die Bindungsaffinität von Wirkstoffen an ihre Zielstrukturen von den gebildeten Wasserstoffbrücken ab. Mit dem neuen Verfahren lässt sich die Stärke dieser zwischenmolekularen Kräfte künftig genau bestimmen.
Das hat laut Thomas Kühne, Professor für Technische Chemie und Leiter der Arbeitsgruppe, Einfluss auf die Chemie, Physik und auch die Materialwissenschaften. „Mit Hilfe dieses neuen Verfahrens lassen sich zukünftig eine ganze Reihe von interessanten Effekten an Grenzflächen wie zum Beispiel Korrosion und Wasserstoffversprödung genauer untersuchen.“