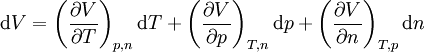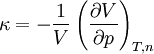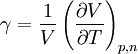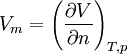Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
ZustandsgleichungAls Zustandsgleichung wird der funktionale Zusammenhang zwischen thermodynamischen Zustandsgrößen bezeichnet, mit deren Hilfe sich der Zustand eines thermodynamischen Systems beschreiben lässt. Dabei wählt man eine der Zustandsgrößen als Zustandsfunktion und die anderen, von ihr abhängigen Zustandsgrößen, als Zustandsvariablen. Zustandsgleichungen werden benötigt, um die Eigenschaften von Fluiden, Fluidgemischen und Feststoffen zu beschreiben. Die bekanntesten Zustandsgleichungen dienen der Zustandsbeschreibung von Gasen und Flüssigkeiten. Der wichtigste und zugleich auch einfachste Vertreter, der in der Regel herangezogen wird, um das Wesen einer Zustandsgleichung zu erklären, ist die allgemeine Gasgleichung. Diese beschreibt zwar nur ein ideales Gas exakt, kann jedoch bei niedrigen Drücken und hohen Temperaturen auch als Näherung für reale Gase herangezogen werden. Bei hohen Drücken, niedrigen Temperaturen und insbesondere Phasenübergängen versagt sie jedoch, so dass andere Zustandsgleichungen notwendig werden. Zustandsgleichungen realer Systeme sind dabei immer Näherungslösungen und können die Eigenschaften eines Stoffes nicht exakt für alle Bedingungen beschreiben. Zustandsgleichungen sind keine Folgerungen aus den allgemeinen Hauptsätzen der Thermodynamik. Sie müssen empirisch oder mittels statistischer Methoden gefunden werden. Sind alle Zustandsgleichungen eines thermodynamischen Systems bekannt bzw. umfasst eine Zustandsgleichung alle Zustandsgrößen des Systems, so können mit Hilfe der Hauptsätze der Thermodynamik alle thermodynamischen Eigenschaften desselben ermittelt werden. In der Thermodynamik wird zwischen kalorischen und thermischen Zustandsgleichungen unterschieden. Aufgrund des zweiten Hauptsatzes der Thermodynamik sind diese jedoch voneinander abhängig. Produkt-Highlight
Thermodynamischer HintergrundZustandsgleichungen stellen einen stoffspezifischen Zusammenhang zwischen thermodynamischen Zustandsgrößen dar. Ein thermodynamisches System, welches aus einer oder mehreren gasförmigen, flüssigen oder festen Phasen besteht, ist im thermodynamischen Gleichgewicht durch eine gewisse Anzahl von Zustandsgrößen eindeutig bestimmt. Zustandsgrößen hängen nur vom aktuellen Zustand, aber nicht von der Vorgeschichte des Systems ab. Zwei Zustände sind genau dann gleich, wenn alle entsprechenden Zustandsgrößen übereinstimmen. Solche Zustandsgrößen sind z. B. die Temperatur T, der Druck p, das Volumen V und die Innere Energie U. Bei einem Stoffgemisch aus K verschiedenen Komponenten sind die Stoffmengen ni (i = 1...K) gleichfalls Zustandsgrößen, wobei statt der einzelnen Stoffmengen meist die gesamte Stoffmenge n = n1 + ... + nK und die Molenbrüche xi = ni / n zur Beschreibung verwendet werden. Die Zustandsgrößen eines Systems sind nicht alle voneinander unabhängig. Die Zahl der unabhängig veränderbaren Zustandsgrößen, d. h. die Zahl F der Freiheitsgrade, hängt von der Zahl K der Komponenten und der Zahl P der verschiedenen Phasen des thermodynamischen Systems ab und ist gegeben durch die Gibbssche Phasenregel: F = K + 2 − P . Bei einem einkomponentigen einphasigen System (z. B. flüssiges Wasser) genügen demnach zwei Zustandsgrößen zur eindeutigen Festlegung des Zustandes, und bei gegebener Stoffmenge n sind die Zustandsgrößen T, p und V nicht unabhängig voneinander. Sind z. B. die Temperatur T und der Druck p vorgegeben, so stellt sich automatisch ein bestimmtes Volumen V ein, das nicht variiert werden kann, ohne zugleich T oder p zu ändern. Befinden sich bei einem einkomponentigen System zwei Phasen im Gleichgewicht, dann genügt bereits eine Zustandsgröße zur Festlegung. Ist z. B. die Temperatur gegeben, dann stellt sich im Phasengleichgewicht zwischen Flüssigkeit und Dampf automatisch ein bestimmter stoffspezifischer Druck ein, der als Dampfdruck bezeichnet wird. Der funktionale Zusammenhang zwischen Temperatur und Dampfdruck ist eine Zustandsgleichung. Ein funktionaler Zusammenhang zwischen Temperatur T, Druck p, Volumen V und Stoffmenge n stellt eine thermische Zustandsgleichung dar. Die meisten thermischen Zustandsgleichungen enthalten den Druck explizit:
Ist das molare Volumen ν(T,p) oder die Dichte ρ(T,p) in Abhängigkeit von Temperatur T und Druck p gegeben, so entspricht dies einer thermischen Zustandsgleichung, die das Volumen explizit enthält: wobei M die mittlere molare Masse des Systems bezeichnet. Alle diese Formen sind gleichwertig und enthalten dieselbe Information. Die Eigenschaften eines thermodynamischen Systems, also die stoffspezifischen Zusammenhänge aller Zustandsgrößen, sind durch eine thermische Zustandsgleichung allein nicht vollständig bestimmt. Die Bestimmung der thermodynamischen Potentiale, welche alle Informationen über ein thermodynamisches System enthalten, erfordert zusätzlich eine kalorische Zustandsgleichung, also die Kenntnis einer von der thermischen Zustandsgleichung unabhängigen Zustandsgröße in Abhängigkeit von der Temperatur. Besonders gebräuchlich ist die einfach messbare spezifische Wärmekapazität H0 bezeichnet die Normalbildungsenthalpie und S0 die Normalentropie pro Mol (T0 = 298,15 K ; p0 = 1,01325 bar), die für viele Stoffe tabelliert sind. Daraus ergibt sich die spezifische freie Enthalpie bei Normaldruck in Abhängigkeit von der Temperatur: Mit der Dichte ρ(T,p) in Abhängigkeit von Temperatur T und Druck p, also einer thermischen Zustandsgleichung, kann daraus die spezifische freie Enthalpie für beliebige Werte ihrer Variablen T und p berechnet werden: Da die freie Enthalpie bezüglich der Variablen T und p ein thermodynamisches Potential ist, sind damit alle thermodynamische Größen des Systems bestimmt und berechenbar. Die kalorische ZustandsgleichungDie kalorische Zustandsgleichung, auch als Energiegleichung bezeichnet, beschreibt die Verknüpfung der inneren Energie U bzw. der Enthalpie H mit jeweils drei thermodynamischen Zustandsgrößen, dem Volumen V (bzw. dem Druck p), der Temperatur T und der Stoffmenge n. Es handelt sich um eine besondere Schreibweise des Ersten Hauptsatzes der Thermodynamik. Für U = U(T,V,n1,...,nk) und H = H(T,p,n1,...,nk) ergeben sich die totalen Differentiale: Mit der Annahme dni = 0 (konstante Stoffmenge) und den Beziehungen folgt wobei CV die isochore Wärmekapazität ist. Die thermische ZustandsgleichungDie thermische Zustandsgleichung setzt die Zustandsgrößen Druck p, Volumen V, Temperatur T und Stoffmenge n zueinander in Beziehung. Für V = V(T,p,n) ergibt sich das totale Differential: Dieses lässt sich vereinfachen durch die Kompressibilität κ, den Volumenausdehnungskoeffizienten γ und das molare Volumen Vm: woraus resultiert: Beispiele für thermische Zustandsgleichungen sind die allgemeine Gasgleichung und die Van-der-Waals-Gleichung. Beispiele für Zustandsgleichungen
Siehe auchFundamentalgleichung, Freiheitsgrad, Phasendiagramm, Gibbssche Phasenregel, Maxwell-Beziehung, Andrews-Diagramm, Zustandsänderung, Taitsche Gleichung Kategorien: Zustandsgleichung | Thermodynamik |
|
| Dieser Artikel basiert auf dem Artikel Zustandsgleichung aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. |





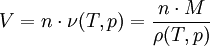
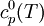 bei Normaldruck
bei Normaldruck 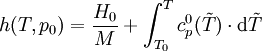
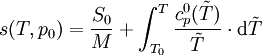
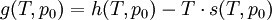
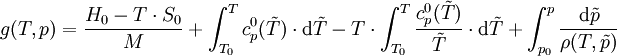
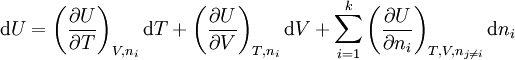
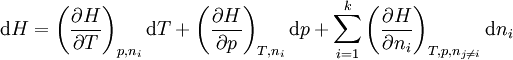
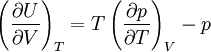
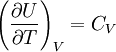
![\mathrm d U = \left[ T \left( {\partial p \over \partial T} \right)_{V} - p \right] \mathrm d V + C_V \mathrm d T](images/math/3/d/4/3d403f20f042ab1b6eb25cf6dcf2cedc.png)