„Frustrierte“ Ionen für die Feststoffbatterie
Anzeigen
Ein internationales Team mit TU Graz-Beteiligung präsentiert einen neuen Festelektrolyten für Batterien: Er zeigt einen der schnellsten je gemessenen Lithium-Wanderungsprozesse in einem Lithium-Ionenleiter.

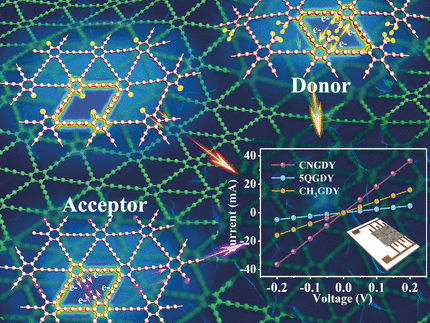
Eine neue Klasse von Festelektrolyten für die Feststoffbatterie von morgen: kristallin, aber in der Ionenbeweglichkeit ähnlich wie Flüssigelektrolyte.
© Lunghammer - TU Graz
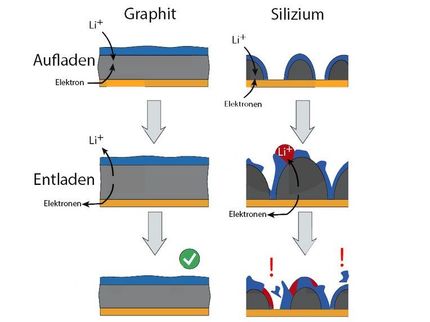
Festkörperbatterien sind die zurzeit vielversprechendste Technologie, um der Elektromobilität zum Durchbruch zu verhelfen. Batterien mit festen Elektrolyten, in denen sich Lithium-Ionen zwischen den Elektroden bewegen, sind somit der „heilige Gral“ der Festkörperbatterieforschung. Die Vorteile von solchen Systemen gegenüber aktuellen Lithium-Ionenbatterien mit flüssigen Elektrolyten liegen auf der Hand: Sie haben eine höhere Energiedichte und sind aufgrund ihrer nicht entflammbaren Komponenten deutlich sicherer.
Was bislang jedoch fehlte, waren geeignete Materialien mit einer ähnlich hohen Ionenleitfähigkeit wie sie flüssige Elektrolyte besitzen. Gemeinsam mit Kollegen der TU München und der belgischen Université Catholique de Louvain stellten Forscher der TU Graz nun im Fachjournal Chem einen vielversprechenden kristallinen Ionenleiter mit bemerkenswert hoher Lithium-Ionenmobilität vor; die gemessenen Diffusionskoeffizienten übertreffen die aktuellen Spitzenkandidaten.
Ionen auf vergeblicher Platzsuche
Der neue Ionenleiter mit der Summenformel LiTi2(PS4)3 ist ein Lithium-Titanthiophosphat, daher die Abkürzung LTPS. LTPS zeigt eine ungewöhnliche Kristallstruktur, die sich durch sogenannte „geometrische Frustration“ auszeichnet. Im Gegensatz zu anderen Ionenleitern bietet die Kristallstruktur von LTPS keine energetisch stark begünstigten Verweilplätze für die Ionen. Sie sind daher nie mit ihrem aktuellen Platz zufrieden und unterliegen somit einer Frustration. Berechnungen der Gruppe um Geoffroy Hautier von der belgischen Université catholique de Louvain zeigen, dass diese Frustration der Ionen zu einer sehr hohen Lithium-Beweglichkeit führt.
„Die Lithium-Ionen suchen mehr oder weniger ‚verzweifelt‘ einen geeigneten Platz und bewegen sich dabei sehr rasch durch die kristallographische Struktur von LTPS. Genau diese hohe Ionenbeweglichkeit wollen wir in Elektrolytkörpern für Feststoffbatterien haben“, erklärt Martin Wilkening vom Institut für Chemische Technologie von Materialien der TU Graz und Leiter des ebendort angesiedelten Christian Doppler Labors für Lithium-Batterien.
Tempo auch bei Tiefsttemperaturen
Wilkenings Team konnte dieses errechnete hohe Beweglichkeitsmaß der Ionen mit Kernresonanzmethoden experimentell bestätigen. Martin Wilkening dazu: „Wir fanden deutliche Hinweise auf zwei Sprungprozesse, die die Ergebnisse der Rechnungen vollends unterstützen. In der Struktur von LTPS können die Lithium-Ionen auf ringförmigen Pfaden hin- und her-, sowie von einem Ring zum nächsten springen. Der letzte Schritt, der Inter-Ring-Prozess, ermöglicht den langreichweitigen Ionentransport.“
Selbst unter kryogenen Bedingungen – also bei extrem niedrigen Temperaturen – konnten die Intra-Ring-Hüpfprozesse der Lithium-Ionen noch nicht vollständig ausgeschaltet werden. Die Lithium-Ionen sind auch bei 20 Kelvin (minus 253 Grad Celsius) auf der Sensitivitätsskala der Kernresonanzspektroskopie noch mobil und suchen nach der passenden Potentialmulde in der sehr flachen Energielandschaft von LTPS. Ein derartiges Verhalten ist äußerst selten, so Wilkening: „Sinkt die Temperatur, wird den Ionen die thermische Energie genommen und ihre Mobilität nimmt deutlich ab. Es ist bemerkenswert, dass wir in LTPS aber sogar noch bei solch niedrigen Temperaturen Ionenmobilität feststellen. Das zeigt, wie stark der Bewegungsdrang der Ionen in LTPS ist.“ Die Betriebstemperatur einer Feststoffbatterie, beispielsweise im Elektrofahrzeug, wird selbstverständlich gar nie so niedrig sein.
Vertreter einer neuen Materialklasse
LTPS ist mit diesem superschnellen Diffusionsprozess, dessen Ursache energetische Frustration ist, ein Vertreter einer neuen Klasse von Festelektrolyten. Diese sind zwar kristallin, besitzen aber Bewegungseigenschaften, die eher jenen von Flüssigelektrolyten ähneln. Die Entdeckung und experimentelle Untersuchung von LTPS ist nun der Startpunkt für die Suche nach weiteren Verbindungen, in denen ein ähnlicher Leitungsmechanismus vorherrscht.
Die Studie wurde in Zusammenarbeit mit Toyota erstellt. Die UCLouvain hat die Entdeckung von LTPS zum Patent eingereicht.
Kooperationspartner (in alphabetischer Reihenfolge):
- Toyota Motor Europe
- TU Graz
- TU München
- Université catholique de Lou
Originalveröffentlichung
Weitere News aus dem Ressort Wissenschaft
Diese Produkte könnten Sie interessieren
Meistgelesene News
Weitere News von unseren anderen Portalen
Verwandte Inhalte finden Sie in den Themenwelten
Themenwelt Batterietechnik
Die Themenwelt Batterietechnik bündelt relevantes Wissen in einzigartiger Weise. Hier finden Sie alles über Anbieter und deren Produkte, Webinare, Whitepaper, Kataloge und Broschüren.

Themenwelt Batterietechnik
Die Themenwelt Batterietechnik bündelt relevantes Wissen in einzigartiger Weise. Hier finden Sie alles über Anbieter und deren Produkte, Webinare, Whitepaper, Kataloge und Broschüren.