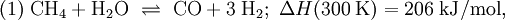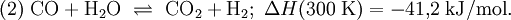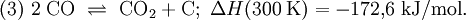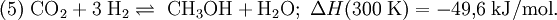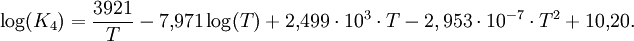Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Methanol
Methanol ist ein einwertiger Alkohol, der sich vom einfachsten Alkan Methan durch Ersetzung eines Wasserstoffatoms durch die Hydroxylgruppe ableitet. In der Natur kommt er in Baumwollpflanzen, Heracleum-Früchten, Gräsern und in ätherischen Ölen vor. Methanol entsteht auch bei Gärungsvorgängen, z. B. von Zuckerrohrsaft. Bei der Vergärung von Früchten können die darin enthaltenen Pektine u. a. zu Methanol abgebaut werden. In käuflichen alkoholischen Getränken wird aber kaum Methanol gefunden, da Prozessführung, Destillation sowie Lebensmittelkontrolleure für ein hohes Maß an Sicherheit sorgen. Weiteres empfehlenswertes Fachwissen
GeschichteSchon in der Antike benutzten die Ägypter zur Balsamierung ihrer Toten ein Substanzgemisch, das unter anderem Methanol enthielt. Im Jahr 1661 konnte Robert Boyle das Methanol aus Holzessig gewinnen. Elementaranalytische Methoden waren in diesem frühen Stadium der Chemie jedoch noch nicht entwickelt. 1834 wurde schließlich die elementare Zusammensetzung von Methanol von den französischen Chemikern Jean Baptiste Dumas und Eugene Peligot geklärt. Sie gaben der Substanz den Namen „methylene“. Methylene ist eine Zusammensetzung aus den griechischen Worten méthy (Wein) und hylé (Holz). Die ersten großtechnischen Methanolsynthesen erfolgten durch eine trockene Destillation von Holz. Noch im Jahr 1930 wurde in den USA 50 % des Methanols nach diesem Verfahren gewonnen. 1923 entwickelte Matthias Pier für die BASF einen Prozess, um aus Kohle und Wasserstoff Methanol zu synthetisieren. 1923 begann die erste Großproduktion in den Leuna-Werken, dem Ammoniakwerk Merseburg. Dieser Prozess basierte auf einem Zink-Chrom-Katalysator, extrem hohen Drücken und Temperaturen. In modernen Methanolsynthesen werden effizientere Katalysatoren eingesetzt, welche die Verwendung von moderateren Temperaturen und Drücken erlauben. Von der Firma ICI wurde im Jahr 1966 die erste Niederdrucksynthese mit einem Kupferoxid-Zinkoxid–Aluminium-Katalysator durchgeführt. Fast alle späteren Niederdruckkatalysatoren nutzten ebenfalls die preisgünstigen Grundstoffe Kupfer, Zink, Aluminium. Die Mehrzahl der Anlagenneubauten seit den siebziger Jahren erfolgte dann für das Niederdruckverfahren; sie nutzen als Ausgangsstoff fast ausschließlich Erdgas. HerstellungGrundlagenHistorisch wurde Methanol schon im 17. Jahrhundert durch trockene Destillation (= Erhitzen unter Luftabschluss, Pyrolyse) von Laubholz (daher der Trivialname Holzgeist) gewonnen. Im Holzdestillat befanden sich etwa 1,5 - 3 % Methanol, 10 % Essigsäure, 0,5 % Aceton, Essigsäuremethylester, Acetaldehyd, Holzteer und im Gasgemisch Wasserstoff, Kohlenstoffmonoxid und Ethen. Heutzutage wird Methanol großtechnisch aus Synthesegas hergestellt. Als Nebenprodukte fallen Ethanol und Dimethylether an. Die Weltjahresproduktion lag im Jahr 2005 bei circa 30 Mio t. Die größten Hersteller sind die Methanex Corporation mit einer Jahresproduktion von 5,3 Mio t mit Sitz in Vancouver, Kanada, und die Methanol Holdings (Trinidad) Ltd. in Trinidad mit einer Produktionsmenge von 4 Mio t/a (Stand 2005).[1][2] Die aktuellen Verfahren zur Herstellung von Methanol unterscheiden sich durch den Reaktionsdruck. Die Verfahren können wie folgt klassifiziert werden:
Am wichtigsten ist das Niederdruckverfahren, das in der Regel bei 230-250 °C ausgeführt wird. Als Rohstoffe für die Methanolherstellung können Erdgas, Benzin, Rückstandsöle der Erdölaufarbeitung, Kohle oder auch Kohlenstoffdioxid und Wasserstoff verwendet werden. Bislang ist der wichtigste Grundstoff das Erdgas. Herstellung von Methanol aus ErdgasErdgas besteht fast vollständig aus Methan. Vor der Reaktion müssen vom Erdgas alle Bestandteile entfernt werden, die den Katalysator für die Reaktion zerstören könnten. Der Schwefelwasserstoffgehalt muss unter 0,1 ppm liegen. Unter katalytischem Einfluss kann sich Methan und Wasserdampf zu Kohlenstoffmonoxid und Wasserstoff umsetzen. Die Reaktion (1) von Methan und Wasser zu Kohlenstoffmonoxid und Wasserstoff ist endotherm, d. h. es muss Energie zugeführt werden, damit der Prozess in Richtung Kohlenstoffmonoxidbildung abläuft. Das Methangas muss auf ca. 420-550 °C vorgeheizt werden und wird dann durch Röhren geleitet, die mit Nickel imprägniert sind. Der Prozess der Umwandlung von Methan zu Kohlenstoffmonoxid und Wasserstoff heißt Reformierung. Da nach Gleichung (1) aus zwei Molekülen vier Moleküle entstehen, begünstigt ein niedriger Druck diese Reaktion (Prinzip von Le Chatelier); Eine Druckerhöhung würde die Rückreaktion in Richtung Methan begünstigen. Das Kohlenstoffmonoxid reagiert nach (2) weiter mit Wasserdampf, so dass sich neben Kohlenstoffmonoxid zusätzlich auch Kohlenstoffdioxid bildet. Hohe Temperaturen begünstigen die Verschiebung des sogenannten Boudouard-Gleichgewichts nach links, welches sich zwischen Kohlenstoffmonoxid auf der linken, Kohlenstoffdioxid und Kohlenstoff auf der rechten Seite einstellt: Für die Bildung von Methanol aus Kohlenstoffmonoxid oder Kohlenstoffdioxid und Wasserstoff können die folgenden Gleichungen formuliert werden: Diese beiden Reaktionen sind exotherm, d. h. die Wärmeentwicklung während der Reaktion kann für die Durchführung der Niederdruckkatalyse bei ca. 250 °C genutzt werden. Nach den Gleichungen entstehen aus drei bzw. aus vier Molekülen eines bzw. zwei. Nach dem Prinzip von Le Chatelier führt also eine Druckerhöhung zu einer Verschiebung des Gleichgewichtes nach rechts. Für die Temperaturabhängigkeit der Gleichgewichtskonstanten der Reaktion (4) gilt die folgende Beziehung: Mit dieser Gleichung lässt sich die Methanolbildung bei verschiedenen Reaktionstemperaturen berechnen. Methanolproduktion in 1000 t:
Herstellung von Methanol aus KohleIn diesem Verfahren wird Kohle unter Hitze und Zugabe von Luftsauerstoff vergast (Kohledruckvergasung). Nach Kühlung des entstandenen Synthesegases (CO + 2 H2) werden die Teerabscheidungen entfernt und die schwefelhaltigen Verunreinigungen, die in der Kohle beträchtlich höher sind als im Erdgas, mit dem Rectisolverfahren entfernt. Der weitere Prozess verläuft analog der Darstellung aus Erdgas. Aufgrund der guten Verfügbarkeit und des geringen Preises von Erdgas und der günstigeren Anlagekosten wurden kaum neue Anlagen auf Kohlebasis errichtet. 1977 lagen beispielsweise die Kosten des Baus einer Anlage zur Methanolsynthese inklusive aller Nebenanlagen mit einer Kapazität von 2500 t/d bei 435 Mio. DM für Verfahren basierend auf Kohle, die Kosten einer Syntheseanlage aus Erdgas jedoch bei nur 171 Mio. DM. LPMEOH-VerfahrenIn den USA wurde Anfang der achtziger Jahre ein Programm „Saubere Kohle-Technologie“ (Clean Coal Technology = CCT) zur Verbesserung von Kohletechnologien aufgelegt. Dieses Programm hatte zum Ziel, die Kohlenstoffdioxidemissionen bei der Kohlevergasung drastisch zu senken. Im Zusammenhang mit dem Projekt wurde eine Anlage zur Methanolherstellung (LPMEOH-Verfahren[3]) aus Synthesegas von den Firmen Eastman Chemical Company und Air Products entwickelt. Schon im Jahre 1983 errichtete Eastman Chemical Company in Kingsport, Tennessee, eine Kohlevergasungsanlage. Mit dieser Anlage können 1000 Tonnen Kohle pro Tag in Synthesegas umgewandelt werden. Die erste LPMEOH-Anlage wurde zwischen Oktober 1995 und Januar 1997 fertiggestellt. Im LPMEOH-Reaktor befindet sich der Katalysator in einem hochsiedendem Mineralöl (30 % Katalysator auf 70 % Mineralöl). In den Reaktor wird nun von unten Synthesegas eingeleitet. Bei ca. 235 °C bildet sich im Reaktor Methanol, das in Dampfform zusammen mit dem nicht umgesetzten Synthesegas den Reaktor wieder verlässt. Nach Abkühlung, Abtrennung und Reinigung durch Destillation erhält man reines Methanol. Der Katalysator verliert pro Tag etwa 0,2 % an Aktivität und muss nach längerem Gebrauch ersetzt werden. In der Anfangsphase wurden 260-300 Tonnen Methanol/Tag hergestellt. Die Baukosten für die LPMEOH-Anlage wurden mit 214 Millionen Dollar angegeben, die Herstellungskosten pro Gallone Methanol aus Kohle mit 0,50 $. Dies entspricht etwa 168 Dollar/Tonne oder 0,168 $/kg. Nach Angaben des Chemieanlagenherstellers Lurgi[4] liegen die Herstellungskosten von Methanol auf der Basis von Erdgas derzeit zwischen 50-110 US-$/Tonne. AusblickDem Chemiker und Nobelpreisträger George Olah zufolge sind mittlerweile Verfahren entwickelt, mit denen Methanol direkt und ohne Synthesegas aus Methan hergestellt werden kann. Des Weiteren, so Olah, könne man Methanol auch aus CO2 und Wasser unter Zuführung von elektrischem Strom herstellen; so sei ein „Recycling“ von CO2 möglich.[5]. (Vergleiche auch Methanolwirtschaft). Auf diesem Gebiet liegt bereits eine Vielzahl von Patenten vor, die aufzeigen, dass dies möglich ist. Das gegenwärtige Problem besteht darin, die notwendigen hohen Stromdichten für eine Großproduktion zu erzielen. Wirtschaftlich und energiepolitisch sind solche Verfahren jedoch äußerst fragwürdig, weil für das CO2-Recycling mehr Energie aufgebracht werden müsste als bei der vorhergehenden Verbrennung von C zu CO2 gewonnen würde. Japanische Wissenschaftler haben inzwischen einen verbesserten Katalysator für die Methanolsynthese entwickelt (Patentschrift DE 69808983 T2)[6]. Die Wissenschaftler beobachteten einen zwei- bis dreifach höheren Umsatz gegenüber herkömmlichen Katalysatoren bei der Umsetzung von Kohlenstoffdioxid und Wasserstoff zu Methanol. Sie heben in ihrer Patentschrift hervor, dass es mit verbesserten Katalysatoren möglich sein sollte, die globale Erwärmung durch Kohlenstoffdioxid zu lindern. Dazu bietet sich die CO2-Sequestrierung an. Ein Kohlekraftwerk mit 1000 MW Leistung setzt pro Jahr 6 Millionen Tonnen Kohlenstoffdioxid frei. Um die 15 % Kohlenstoffdioxid aus dem Rauchgas abzutrennen, könnte der Schornstein durch einen Waschturm, gefüllt mit einer organischen Stickstoffverbindung, ersetzt werden. Beim Durchleiten von Kohlenstoffdioxid bilden sich dann Carbaminsäuren. Das Kohlenstoffdioxid lässt sich in einem zweiten Arbeitsgang in reiner Form durch Erhitzen der Carbaminsäuren gewinnen; dabei wird das Amin wieder regeneriert. Ein derartiges Verfahren wird bereits zur Abtrennung von Kohlenstoffdioxid aus Erdgas genutzt. Wasserstoff kann durch Elektrolyse von Wasser oder durch starke Erhitzung von Wasserdampf und Abtrennung des Wasserstoffs erzeugt werden. Ob die Gewinnung des Kohlenstoffdioxids (zum Einsatz für die Methanolsynthese) aus Abgasen oder aus der Luft jedoch wirtschaftlich ist, bleibt fraglich. Chemische EigenschaftenAuf Grund der polaren Hydroxylgruppe lässt sich Methanol mit Wasser in jedem Verhältnis mischen. Die Ähnlichkeit zu Wasser zeigt sich auch im Lösungsvermögen von einigen Mineralsalzen in Methanol (Calciumchlorid, Kupfersulfat). Es ist ferner in Diethylether und anderen organischen Lösungsmitteln (auch in Kohlenwasserstoffen unter Wasserausschluss) gut löslich. Nicht löslich ist Methanol in Fetten und Ölen. Methanol verbrennt mit blauer, fast unsichtbarer Flamme. Der Flammpunkt liegt bei 11 °C. Methanoldämpfe bilden mit Luft explosionsfähige Gemische. Die UN-Nummer von Methanol ist 1230, die Gefahrnummer 336. Methanol hat einen Spezifischen Heizwert von 19.700 kJ·kg−1 und eine Energiedichte von 4,4 kWh·l−1. AnwendungAls KraftstoffMethanol kann in mindestens vier verschiedenen Varianten als Kraftstoff eingesetzt werden:
In der ChemieMethanol ist einer der wichtigsten Ausgangsstoffe für Synthesen in der chemischen Industrie. Es wird vor allem für folgende Produkte bzw. Reaktionen verwendet (nach der eingesetzten Menge geordnet):
Sonstige AnwendungenMethanol findet als Lösungs- und Frostschutzmittel Einsatz. Ebenso findet es Anwendung bei der Sensorreinigung von digitalen Spiegelreflexkameras, da es keine Schlieren hinterlässt und rückstandslos verdunstet. NachweisOrganoleptisch: Methanol hat einen unverwechselbaren, nicht alkoholischen, jedoch süßlichen Geruch wie z. B. Ethanol (Weingeist). Wird Methanol mit Borax vermischt und angezündet, verbrennt das dabei entstehende Trimethylborat mit intensiv grüner Flamme. Diese Reaktion funktioniert mit ähnlichem Ergebnis, aber weniger intensiver Grünfärbung auch mit Ethanol, allerdings nur mit einem Zusatz von konzentrierter Schwefelsäure. Deswegen können Ethanol und Methanol mit dieser so genannten Boraxprobe unterschieden werden. GiftigkeitMethanol selbst ist nur von geringer Toxizität, wohl giftig sind aber seine Metabolite, so der durch die Alkoholdehydrogenase (ADH) gebildete Formaldehyd und die daraus entstehende Ameisensäure. Insbesondere letztere führt nach einer häufig symptomlosen Latenzzeit von 6 bis 30 Stunden nach Methanolaufnahme zur Ausbildung einer metabolischen Azidose. Ameisensäure wird vom menschlichen Stoffwechsel nur sehr langsam abgebaut und sammelt sich so während des vergleichsweise zügigen Abbaus des Methanols im Körper an. Dosen von 0,1 g Methanol pro kg Körpergewicht sind gefährlich, über 1 g pro kg Körpergewicht lebensbedrohlich. Die Vergiftungssymptome einer Methanolintoxikation verlaufen in drei Phasen. Direkt nach Aufnahme von Methanol zeigt sich wie beim Ethanol ein narkotisches Stadium, die berauschende Wirkung ist jedoch geringer als bei Ethanol. Nach der häufig asymptomatischen Latenzphase treten Kopfschmerzen, Schwächegefühl, Übelkeit, Erbrechen, Schwindel, beschleunigte Atmung auf - die Folgen der sich ausbildenden metabolischen Azidose. Charakteristisch ist die Schädigung von Nerven, insbesondere am Auge. Netzhautödeme bedingen ein nur noch verschwommenes Sehen und können zur irreversiblen Erblindung führen. Der Tod kann als Folge einer Atemlähmung eintreten. Die Behandlung einer Methanolintoxikation erfolgt über eine Unterbindung des Methanolmetabolismus, z. B. durch Ethanolgaben (0,7 g Ethanol pro kg Körpergewicht), wodurch der Methanolabbau kompetitiv gehemmt wird, bzw. durch Gaben des ADH-Inhibitors 4-Methylpyrazol (Fomepizol). Der Ameisensäureabbau kann durch Folsäuregaben gefördert werden. Einer Azidose kann durch Darreichung von Natriumhydrogencarbonat begegnet werden; ggf. wird eine Hämodialyse notwendig. Die Behandlung ist bis zum Absinken des Blutmethanolgehaltes unter einen bestimmten Grenzwert notwendig. Methanol entsteht regelmäßig als Nebenprodukt bei der alkoholischen Gärung und reichert sich in Destillaten, z. B. bei der Herstellung von Spirituosen, an. Daher wird bei der Destillation die Methanolfraktion abgetrennt. Um diese Abtrennung so vollständig wie möglich zu gestalten, sind große Sorgfalt und Erfahrung sowie ein strenges Temperaturregime vonnöten. Minderwertige Spirituosen können beträchtliche Mengen Methanol enthalten, welche bei übermäßigem Genuss bedenklich sind. In der Raumluft konnten Arbeiter 20-25 ppm Methanol ohne gesundheitliche Folgewirkungen auch noch nach zwei Jahren vertragen. Methanolkonzentrationen von über 200 ppm führen nach längerer Einatmung zu Kopfschmerzen. Konzentrationen von 500-1100 ppm wurden von freiwilligen Versuchspersonen nur 3-4 Stunden ertragen. Methanol wird auch über die Haut sehr gut resorbiert. Quellen
http://webbook.nist.gov/cgi/cbook.cgi?ID=67-56-1&Units=SI&cTC=on Siehe auchDMFC, Brennstoffzelle, Dimethylterephthalat Kategorien: Giftiger Stoff | Feuergefährlicher Stoff | Alkohol |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dieser Artikel basiert auf dem Artikel Methanol aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||