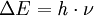Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
SpektroskopieSpektroskopie ist eine Gruppe experimenteller Verfahren, die anhand des Spektrums (Farbzerlegung) von Lichtquellen untersuchen, wie elektromagnetische Strahlung und Materie in Wechselwirkung stehen. Sie sind wichtige Analysemethoden der Physik, Chemie und Astronomie und gehen auf eine 1859 von Kirchhoff und Bunsen gemachte Entdeckung zurück, dass verschiedene chemische Elemente die Flamme eines Gasbrenners auf charakteristische Weise färben. Zuvor hatte bereits Joseph von Fraunhofer 1814 im Spektrum der Sonne auftretende dunkle Linien untersucht, ohne allerdings ihren Ursprung erklären zu können. Spektroskopische Beobachtungen gaben entscheidende Impulse für die Entwicklung der Quantenmechanik. Man unterscheidet drei Fälle der Wechselwirkung:
Im allgemeineren Sinne wird die Bezeichnung Spektroskopie auch für die Messung der Energieverteilung von z. B. Gammastrahlung oder Teilchenstrahlungen wie Alpha-, Beta-Strahlung oder freien Neutronen gebraucht. Weiteres empfehlenswertes Fachwissen
Spektroskopie im engeren Sinnbezieht sich meistens auf den letzteren Fall. Man untersucht, bei welchen Frequenzen oder Wellenlängen eine Substanz Energie in Form von Lichtquanten bzw. elektromagnetischen Wellen aufnehmen (absorbieren) oder abgeben (emittieren) kann. Die Energie eines Lichtquants oder die dementsprechende Frequenz einer elektromagnetischen Welle entspricht dabei der Energiedifferenz zweier quantenmechanischer Zustände der zu untersuchenden Substanz:
Darin ist h die Planck-Konstante, ν die Frequenz des Lichtquants und ΔE die Energiedifferenz. Diese Gleichung wird auch als Grundgleichung der Spektroskopie bezeichnet. Die Energiedifferenzen quantenmechanischer Zustände hängen von der chemischen Zusammensetzung einer Probe oder der Struktur eines Moleküls ab und enthalten daher wichtige Informationen für den Chemiker, Physiker und Biologen. Historisch bezeichnet der Begriff in erster Linie solche Verfahren, die die Absorption oder Emission von Licht untersuchen. Mit Hilfe eines Spektrometers wird dabei ein Lichtspektrum (Intensität des absorbierten oder ausgestrahlten Lichts in Abhängigkeit von der Wellenlänge) gemessen. Als Spektrum bezeichnet man allgemein eine Auftragung einer zur Energie proportionalen Größe (z.B. Frequenz, Wellenzahl, Kreiswellenzahl) gegen eine Intensität. Der Begriff darf nicht mit Chromatogramm (Retentionsgröße gegen Intensität) in der Chromatographie oder Massenspektrum (Masse gegen Intensität) in der Massenspektrometrie verwechselt werden. Neben dem Bereich des sichtbaren Lichts deckt die Spektroskopie heute einen großen Teil des elektromagnetischen Spektrums ab, von den Radiowellen bis zur Gammastrahlung. Ziel der Spektroskopie ist es, aus dem gemessenen Spektrum Rückschlüsse auf die Probe bzw. den strahlenden Körper zu ziehen - etwa
Physikalische Grundlagen
StrahlungsquellenKlassische SpektroskopieDie Untersuchung der Lichtemission bzw -absorption von Molekülen und Atomen mit Hilfe von Gitter- und Prismenspektrometern sind die ältesten spektroskopischen Verfahren. Sie werden daher auch als Klassische Spektroskopie bezeichnet. Viele der grundlegenden Untersuchungen über den Aufbau des Atoms wurden erst durch die Entwicklung und Anwendung hochauflösender Gitter- und Prismenspektrometer möglich. AstronomieDas Element Helium wurde - lange vor seinem terrestrischen Nachweis auf der Erde - zunächst durch spektroskopische Untersuchungen des Sonnenlichtes erkannt. Als eine bestimmte Spektrallinie auf keinem Wege labor-chemischen Substanzen zugeordnet werden konnte, vermutete man, dass auf der Sonne ein unbekanntes Element existieren müsse. Weitere klassische Erfolge der astronomischen Spektralanalyse bzw. -Spektroskopie sind
Die zugehörigen Messinstrumente ("Spektralapparate") der Astrospektroskopie sind:
MolekülspektroskopieBei der Molekülspektroskopie wird die Wechselwirkung von Molekülen mit elektromagnetischen Feldern untersucht. Dies ermöglicht sowohl die Charakterisierung molekularer Eigenschaften wie Bindungslängen und -stärken, als auch die Identifizierung der atomaren Bestandteile. Die beobachteten Molekülspektren unterscheiden sich von den Atomspektren durch sehr viel mehr, meist überlappende Linien ("Banden"). Ursache dafür ist, dass die Moleküle nicht nur durch Elektronenübergänge, sondern auch bei Schwingungen der Atome gegeneinander und Rotationen des Moleküls um eine seiner Achsen Energie absorbieren bzw. emittieren können. Die grundlegenden Untersuchungen zur Molekularphysik wurden Anfang des letzten Jahrhunderts mit hochauflösenden Gitterspektralapparaten gemacht (siehe z.B. den Artikel Gitterspektrometer). Heute werden hochgenaue Untersuchungen an Molekülen häufig mit laserspektroskopischen Verfahren durchgeführt. Spektroskopiearten nach Wellenlängen und untersuchten Eigenschaften
Spektroskopiearten und -methoden in der Analytik
LiteraturAllgemeine Lehrbücher
Spezielle Werke
Kategorien: Spektroskopie | Physikalisches Analyseverfahren | Analytische Chemie | Physikalische Chemie |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dieser Artikel basiert auf dem Artikel Spektroskopie aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. |