Wie ein gewöhnlicher Zusatzstoff Lithium-Ionen-Batterien einen Schub verleiht
Forscher haben herausgefunden, warum ein gängiger Elektrolytzusatz die Leistung von Batterien mit einer Lithium-Kobalt-Oxid-Kathode so effektiv verbessert
Anzeigen
Nitrile - eine organische Verbindung, bei der ein Kohlenstoffatom dreifach an ein Stickstoffatom gebunden ist - werden üblicherweise der Elektrolytformel für Batterien mit einer Lithium-Kobalt-Oxid-Kathode zugesetzt, wodurch diese Batterien ihrer vollen theoretischen Leistung sehr viel näher kommen. Bis jetzt haben Batterieforscher nicht wirklich verstanden, warum diese Nitrile auf diese Weise funktionieren. Eine Gruppe von Elektrochemikern hat jedoch mit Hilfe fortschrittlicher Mikroskopietechniken die Vorgänge auf molekularer Ebene genauer untersucht und herausgefunden, was vor sich geht, wodurch sich neue Wege für eine noch bessere Batterieleistung eröffnen.

Forscher finden heraus, wie ein gängiger Zusatzstoff Lithium-Ionen-Batterien einen Schub verleiht (Symbolbild).
Computer generated picture
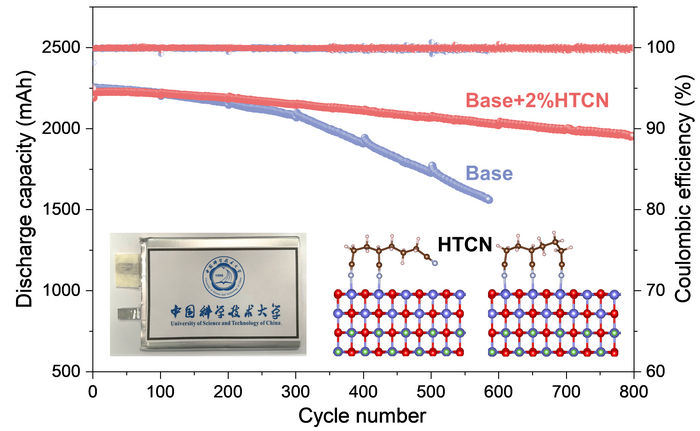
Die elektrochemische Leistung und der Wirkmechanismus des HTCN-Zusatzes auf einer Hochspannungs-LiCoO2-Kathode für praktische Pouch-Zellen werden umfassend untersucht.
Nano Research

Die Studie wurde in der Zeitschrift Nano-Forschung am 22. September 2022 veröffentlicht.
Lithium-Kobalt-Oxid (LiCoO2 oder einfach LCO") ist das am häufigsten verwendete Material für Kathoden - die positiven Elektroden - in Lithium-Ionen-Batterien. Dies gilt insbesondere für Batterien, die in tragbaren elektronischen Geräten verwendet werden, da LCO eine hohe Betriebsspannung, eine hohe Kapazität und eine langfristig stabile Leistung aufweist.
Was LCO-Kathoden jedoch besonders attraktiv macht, ist die Tatsache, dass sie mehr Energie auf kleinerem Raum bieten (höhere Energiedichte), was für kleinere Verbrauchergeräte wie Telefone, Smartwatches und Geräte mit noch engeren Platzverhältnissen wie intelligente Sensoren im Haushalt und in der Industrie sehr nützlich ist.
Zurzeit können LCO-Kathoden jedoch nur etwa die Hälfte ihrer theoretischen spezifischen Kapazität liefern. Im Klartext bedeutet dies, dass die tatsächliche Leistung viel geringer ist als das, was sie theoretisch erzeugen könnten. Daher ist es für sie oft schwierig, die steigenden Anforderungen an die Energiedichte tragbarer Elektronikgeräte zu erfüllen.
Eine Möglichkeit, diese Hürde zu umgehen, wäre die Erhöhung der begrenzten Ladespannung von Batterien mit LCO-Kathoden. Die begrenzte Ladespannung beschreibt den Punkt, an dem eine Batterie als vollständig geladen gilt. Jenseits dieses Punktes könnte die Batterie Schaden nehmen, weshalb sich viele Geräte einfach abschalten, wenn der Grenzwert erreicht ist. Dieser Schwellenwert ist einigermaßen willkürlich festgelegt und könnte daher erhöht werden, und ein solcher Hochspannungsbetrieb bietet die Möglichkeit, die Energiedichte solcher Batterien zu erhöhen.
Hier ergibt sich jedoch ein neues Problem: Der Hochspannungsbetrieb kann schädliche chemische Reaktionen an der Grenzfläche zwischen Kathode und Elektrolyt verstärken. Dies kann zu Rissen und anderen internen Schäden führen, die wiederum die Grenzfläche zwischen den Elektroden weiter verschlechtern können. Letztlich kann all dies zu einer radikalen Abnahme der Batteriekapazität und einer starken Zunahme von Sicherheitsproblemen führen. Die Arbeitstemperatur in diesen Geräten kann aufgrund ihrer eigenen Wärmeentwicklung 45℃ erreichen, was die Lebensdauer der Batterien weiter verkürzt.
Daher hat sich seit einiger Zeit die Beimischung zusätzlicher Verbindungen in die Elektrolytformel, um die Reaktionsaktivität des Elektrolyten (des ionenhaltigen Mediums, das durch die Bewegung positiver und negativer Ionen zur Stromerzeugung beiträgt) an der Grenzfläche zwischen Kathode und Elektrolyt zu verbessern, als sehr wirksame Strategie zur Verringerung der Reaktionsaktivität des Elektrolyten erwiesen.
Es gibt eine Reihe verschiedener Verbindungen, die als solche Elektrolytzusätze verwendet werden, aber für Lithium-Ionen-Batterien sind Nitrile vielleicht die am häufigsten verwendeten. Nitrile sind alle organischen Verbindungen, bei denen ein Teil des Moleküls (eine "funktionelle Gruppe") aus einem Kohlenstoffatom besteht, das dreifach an ein Stickstoffatom gebunden ist.
Die Wirkungsweise von Nitrilzusätzen auf Hochspannungskathoden ist jedoch noch nicht vollständig geklärt, insbesondere bei den praktischen, alltäglichen Hochspannungs-LCO-Batterien. (Bei Pouch-Batterien handelt es sich um eine Art "weiche" Batterie ohne hartes Metallgehäuse, deren Komponenten stattdessen in einer aluminiumbeschichteten Kunststofffolie eingeschlossen sind, die ein wenig wie ein "Pouch" für Kaugummi oder losen Tabak aussieht. Die 1995 erstmals entwickelten Pouch-Batterien, die eine wesentlich effizientere Raumnutzung ermöglichen, sind aufgrund dieses Konstruktionsvorteils inzwischen eine gängige Wahl für die Hersteller).
Es gibt zwei Haupttheorien, die versuchen, den Mechanismus der Nitrilzusätze zu erklären, aber beide haben erhebliche Mängel in ihrer Erklärungskraft.
"Nitrile funktionieren gut, aber wir wissen nicht wirklich, warum sie gut funktionieren, warum diese stabilisierende Wirkung eintritt. Was genau vor sich geht, bleibt ziemlich rätselhaft", sagt Shuhong Jiao, Elektrochemiker an der University of Science and Technology of China (USTC). "Und wenn wir nicht wissen, warum das, was wir tun, um die Batterien zu verbessern, funktioniert, können wir unsere Bemühungen um weitere Verbesserungen nicht optimieren.
Also nahmen die Forscher ein gängiges Nitril-Elektrolytzusatzmittel, dreizähniges, ligandenhaltiges 1,3,6-Hexanetricarbonitril (oder einfacher HTCN), um zu versuchen, Licht in den Mechanismus von Nitrilen bei der Stabilisierung der Hochspannungskathode einer LiCoO2-Batterie zu bringen.
Während die Batterie in Betrieb war und die Leistung einer entsprechenden Batterie ohne HTCN-Elektrolytzusatz bei weitem übertraf, nutzten die Forscher die Elektronenmikroskopie, um einen genaueren Blick auf die Vorgänge zu werfen, kombiniert mit einer Analyse der Ionen- und Elementzusammensetzung des Systems. Sie stellten fest, dass der HTCN-Zusatz die Bildung von Rissen und die Auflösung von Kobaltionen sehr wirksam verhinderte.
Mit Hilfe der Röntgen-Photoelektronenspektroskopie in Verbindung mit einer Reihe theoretischer Berechnungen fanden sie heraus, dass die HTCN-Moleküle effizient an der LCO-Oberfläche adsorbiert (angeheftet) und in die Grenzfläche zwischen Kathode und Elektrolyt eingebettet werden, was wiederum eine Oxidationsreaktion an der LCO-Oberfläche stark hemmt und somit eine kontinuierliche Zersetzung des Elektrolyten verhindert.
Insgesamt führt dies zu einer wesentlich stabileren Grenzfläche zwischen Kathode und Elektrolyt, wodurch die Zersetzung von Komponenten und die Bildung von Rissen deutlich unterdrückt wird. Es ist diese stabile und dichte Kathoden-Elektrolyt-Struktur, die die Stabilität der Batterie über viele Lade- und Entladezyklen hinweg erhöht.
Da die Forscher nun auf molekularer Ebene verstehen, wie Nitriladditive solche Batterien verbessern, können sie nun nach anderen Elektrolytadditivformulierungen suchen, die eine ähnliche oder bessere Grenzflächenstruktur erzeugen.
Hinweis: Dieser Artikel wurde mit einem Computersystem ohne menschlichen Eingriff übersetzt. LUMITOS bietet diese automatischen Übersetzungen an, um eine größere Bandbreite an aktuellen Nachrichten zu präsentieren. Da dieser Artikel mit automatischer Übersetzung übersetzt wurde, ist es möglich, dass er Fehler im Vokabular, in der Syntax oder in der Grammatik enthält. Den ursprünglichen Artikel in Englisch finden Sie hier.