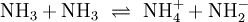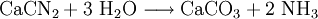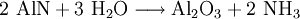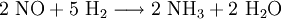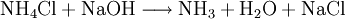Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Ammoniak
Ammoniak ist eine chemische Verbindung von Stickstoff und Wasserstoff mit der Summenformel NH3. Benannt ist es nach dem Ammonssalz Ammoniumchlorid aus der Ammonsoase, heute Oase Siwa. Ammoniak ist ein stark stechend riechendes, farbloses und giftiges Gas, das zu Tränen reizt und erstickend wirkt. Die Dichte von Ammoniakgas ist geringer als die Dichte der Luft. Ammoniak wird mit den UN-Nummern 1005 (gasförmig) bzw. 2073 (wässrige Lösung) bezeichnet. Weiteres empfehlenswertes Fachwissen
Weitere Eigenschaften
Ammoniak-Luft-Gemische sind im Bereich von 15,5 bis 30 Vol.-% Ammoniak explosionsfähig. An heißen Oberflächen ab 630 °C kann es zum Zerfall in Stickstoff und Wasserstoff kommen; diese Zerfallsreaktion wird durch Metalle katalysiert, so dass in großtechnischen Anlagen schon bei Oberflächentemperaturen ab 300 °C die Möglichkeit einer explosionsartigen Zersetzung besteht. Es verbrennt schnell und vollständig, so dass anschließend kein NH3 mehr wahrnehmbar ist. Ammoniak wirkt auf feuchte Körperoberflächen ätzend. Insbesondere feuchte Haut, Schleimhäute, Lungen und Augen werden daher verätzt. Geschluckt ruft es blutiges Erbrechen mit heftigen Schmerzen und eingeatmet Lungenschäden hervor, unter Umständen mit tödlichem Ausgang. Ein Ammoniakgehalt der Luft von 0,5% (5000 ppm) wirkt nach 30 bis 60 Minuten tödlich. Säure-Base-EigenschaftenAmmoniak ist amphoter und bildet als Base unter Protonierung ionische Ammoniumsalze, als Säure mit starken Basen unter Deprotonierung ionische Amide. In flüssigem Ammoniak besteht daher ein Gleichgewicht, das durch ein Ionenprodukt beschrieben werden kann. StrukturDas Ammoniak-Molekül ist nicht eben gebaut, sondern entspricht einer dreiseitigen Pyramide (trigonal-pyramidal). Sie leitet sich von einem Tetraeder ab, in dem das freie (nicht-bindende) Elektronenpaar des Stickstoffs eine Ecke besetzt. Aufgrund der Ladungsabstoßung zwischen den N–H-Bindungselektronen und dem freien Elektronenpaar des Stickstoffs, welches ebenfalls Raum beansprucht, liegen die drei Wasserstoffatome nicht mit dem Stickstoffatom in einer Ebene. Auf diese Weise sind die N–H-Bindungselektronen und das freie Elektronenpaar maximal weit voneinander entfernt. Wegen der höheren Elektronegativität des Stickstoffs gegenüber Wasserstoff und durch die Winkelung ist das Molekül polarisiert: in der Nähe des freien Elektronenpaars liegt eine höhere negative Ladungsdichte vor. Dies ist daher der bevorzugte Angriffsort für Elektrophile, zum Beispiel H+. Bei Raumtemperatur ist das Ammoniakmolekül nicht starr. Das freie Elektronenpaar kann sich auf die gegenüberliegende Seite verlagern, wobei die Wasserstoffatome ebenfalls auf die andere Seite ausweichen. Dadurch kommte es zu einem „Durchschwingen“ des Moleküls, das sich anschaulich mit dem Umklappen eines Regenschirms vergleichen lässt. Diese Eigenschaft trifft auch auf die vom Ammoniak abgeleiteten Verbindungen zu (zum Beispiel Amine), sofern sie nicht durch eine starre Geometrie des Restmoleküls am „Durchschwingen“ gehindert werden. Nachweis
HerstellungDie Herstellung geschieht heute im industriellen Maßstab zum weitaus größten Teil (ca. 90 % der Welterzeugung) aus Wasserstoff und Stickstoff nach dem Haber-Bosch-Verfahren. Alternative Herstellungsverfahren sind die Gewinnung aus Kalkstickstoff (Kalkstickstoffverfahren von Rothe-Frank-Caro) oder durch Hydrolyse von Nitriden (Serpek-Verfahren). Beide Verfahren haben keine nennenswerte technische Bedeutung, da die Synthese nach dem Haber-Bosch-Verfahren billiger ist. Ein weiterer Weg der NH3-Erzeugung ist die Reduktion von Stickstoffmonoxid (NO) mit Wasserstoff (H2). Man kann ihn auch mit Natronlauge aus Salmiaksalz (Ammoniumchlorid) herauslösen (Verdrängungsreaktion; zugleich Nachweisreaktion für Ammoniumsalze) VerwendungAmmoniak ist eines der wichtigsten und häufigsten Produkte der chemischen Industrie. Heute beträgt die Weltjahresproduktion von Ammoniak etwa 125 Millionen Tonnen. Circa 3 % der weltweit produzierten Energie wird für die Herstellung von Ammoniak aufgebraucht. Der Großteil dieser Produktion wird als Ausgangsstoff für Stickstoffdünger verwendet. Daneben wird:
Ammoniak
_________|________________________________
| | |
Oxidation | | sämtlicher
| (NH2)2CO (Harnstoff) weiterer
| / | organischer
Salpetersäure Kunstharze | und
/ / | | \ Düngemittel anorganischer
Nitrate / | | \ Stickstoff
/ | | \ / / | \
Düngemittel / | \ Hydroxylamin / | Nitrile
/ | \ / |
/ Adipinsäure Nitroaromaten Amine Hydrazin
Sprengstoffe \
Anilin(-derivate)
QuellenLiteratur
Kategorien: Giftiger Stoff | Umweltgefährlicher Stoff |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dieser Artikel basiert auf dem Artikel Ammoniak aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||