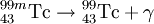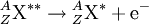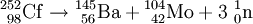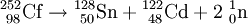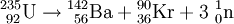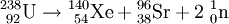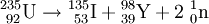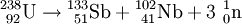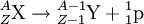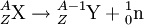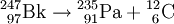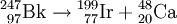Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Radioaktivität
Unter Radioaktivität (von lat. radius, Strahl) oder radioaktivem Zerfall oder Kernzerfall versteht man die Eigenschaft instabiler Atomkerne, sich spontan unter Energieabgabe umzuwandeln. Die freiwerdende Energie wird in Form ionisierender Strahlung, nämlich energiereicher Teilchen und/oder Gammastrahlung, abgegeben. Der historisch geprägte Begriff „Zerfall“ beschreibt in erster Linie die Abnahme des Ausgangsstoffes nach dem Zerfallsgesetz. Diese makroskopische Sichtweise charakterisiert den Vorgang unvollständig. Auf der Ebene der Atome findet eine gesetzmäßig definierte Umwandlung der Kerne statt. Umgangssprachlich wird das Wort Radioaktivität auch für „radioaktive Substanz“ gebraucht. Insbesondere in der öffentlichen Diskussion ist häufig die abgegebene Strahlung oder sogar ionisierende Strahlung aus nicht radioaktiven Quellen gemeint, wenn von Radioaktivität die Rede ist. Weiteres empfehlenswertes Fachwissen
GrundlagenRadioaktiver Zerfall ist kein deterministischer Prozess. Der Zerfallszeitpunkt des einzelnen Atomkerns ist absolut zufällig. Allerdings ist für jedes Nuklid die Zerfallswahrscheinlichkeit pro Zeiteinheit ein fester Wert, der auch durch die Halbwertszeit beschrieben werden kann. Die Halbwertszeit ist der Zeitraum, nach dem durchschnittlich die Hälfte der instabilen Atomkerne einer Menge zerfallen sind. Sie kann Sekundenbruchteile, aber auch einige Milliarden Jahre betragen. Solche langlebigen Nuklide sind beispielsweise Uran-238, Uran-235, Thorium-232 und Kalium-40. Je kürzer die Halbwertszeit, desto größer ist die Aktivität einer gegebenen Substanzmenge. Nicht nur der Zeitpunkt des Zerfalls ist zufällig, sondern unter Umständen auch die Art des Zerfalls. 212Bismut kann beispielsweise mit jeweils unterschiedlicher Wahrscheinlichkeit auf drei verschiedene Arten zerfallen. Eine Nuklidkarte zeigt alle Nuklide mit Arten und Anteilen der möglichen Zerfälle und den Halbwertszeiten. Bei den meisten Zerfallsarten (s. unten) ändert sich die Kernladungszahl (Ordnungszahl) – es entsteht also ein anderes chemisches Element (durch Ausstoß von Protonen, aber immer zusammen mit anderen neutralen Teilchen wie Neutronen) –, bei manchen auch nur die Massenzahl (durch Ausstoß von Neutronen und keinen Protonen). Daneben gibt es Übergänge, bei denen sich nur der Anregungszustand des Kerns ändert (Übergang zwischen verschiedenen Energiezuständen desselben Nuklids). Die Stärke der Radioaktivität wird durch die physikalische Größe Aktivität beschrieben und in der Einheit Becquerel, abgekürzt Bq, angegeben. 1 Bq steht für durchschnittlich einen Zerfall pro Sekunde, ist also eine gegenüber dem früher auch üblichen Curie eine sehr kleine Aktivität. Ein Atomkern ist dann stabil und kann nicht weiter von sich aus zerfallen, wenn es keine Zerfallsart gibt, der zu einem energetisch niedrigeren Zustand führt. Beim Wasserstoff ist dieser Zustand das einzelne Proton als Atomkern, bzw. das Deuteron, das aus Proton und Neutron besteht. Beim Helium enthält das stabile Isotop Helium-3 zwei Protonen und ein Neutron, das stabile Helium-4 zwei Protonen und zwei Neutronen. Beim Lithium und allen schwereren Elementen müssen mindestens gleich viele Neutronen wie Protonen den Kern bilden, damit der Kern stabil ist, und bei schwereren Kernen überwiegen immer mehr die Neutronen. Ab einer gewissen Massenzahl werden alle Atomkerne instabil. Durch Einwirkung von Teilchenstrahlung, insbesondere Neutronenstrahlung (Neutronenaktivierung) können in Kernreaktionen stabile Atomkerne in andere, instabile Atomkerne umgewandelt werden. Geschichte
1896 entdeckte Antoine Henri Becquerel bei dem Versuch, die gerade gefundene Röntgenstrahlung durch Fluoreszenz erklären zu wollen, dass Uransalz fotografische Platten zu schwärzen vermochte. Allerdings war die Uranprobe dazu auch ohne Vorbelichtung in der Lage, was Fluoreszenz als Ursache ausschloss. Wie er später zeigte, konnte diese neue Strahlung lichtundurchlässige Stoffe durchdringen und Luft ionisieren, ohne dabei von Temperaturänderungen oder chemischen Behandlungen der Probe beeinflusst zu werden. Weitere radioaktive Elemente fanden Marie und Pierre Curie 1898 mit Thorium sowie zwei neuen um ein Vielfaches stärker strahlenden Elementen, die sie Radium und Polonium tauften. Durch Untersuchung des Durchdringungsvermögens gelang es Ernest Rutherford 1899, zwei Strahlungskomponenten zu unterscheiden. Stefan Meyer und Egon Schweidler sowie Friedrich Giesel konnten noch im gleichen Jahr zeigen, dass diese in magnetischen Feldern in unterschiedliche Richtungen abgelenkt werden. Eine dritte Komponente, die sich nicht durch Magnetfelder ablenken ließ und ein sehr hohes Durchdringungsvermögen aufwies, wurde 1900 von Paul Ulrich Villard entdeckt. Für die drei Strahlungsarten prägte Rutherford die Bezeichnungen Alpha-, Beta- und Gammastrahlung. Bis 1909 hatte sich erwiesen, dass Alphastrahlung aus Heliumkernen und Betastrahlung aus Elektronen besteht. Die Vermutung, dass es sich bei Gammastrahlung um eine elektromagnetische Welle handelt, konnte erst 1914 von Rutherford und Edward Andrade gezeigt werden. Bereits 1903 – 6 Jahre bevor man von Atomkernen wusste – entwickelten Rutherford und Frederick Soddy eine Hypothese, nach der die Radioaktivität mit der Umwandlung von Elementen verknüpft sei. Davon ausgehend formulierten 1913 Kasimir Fajans und Frederick Soddy die so genannten radioaktiven Verschiebungssätze. Diese beschreiben die Änderung von Massen- und Ordnungszahl beim Alpha- und Betazerfall, womit die natürlichen Zerfallsreihen als eine schrittweise Abfolge von diesen Zerfallsprozessen erklärt werden konnten. Irène und Frédéric Joliot-Curie gelang es 1933 erstmals, radioaktive Elemente künstlich zu erzeugen. Durch den Beschuss von Proben mit α-Teilchen konnten sie neue Isotope herstellen, die aufgrund ihrer kurzen Halbwertszeiten in der Natur nicht vorkommen. Bei ihren Versuchen entdeckten sie 1934 eine neue Art des Betazerfalls, bei dem Positronen anstelle von Elektronen abgestrahlt werden. Seither unterscheidet man zwischen β+- und β−-Strahlung. Zerfallsarten
Radioaktive Kerne können auf verschiedene Weise zerfallen, je nach ihrer Zusammensetzung aus Protonen und Neutronen. Historisch besonders bedeutsam sind die Zerfallsarten Alpha-, Beta- und Gammazerfall. Sie wurden als erste entdeckt und sind die bei weitem am häufigsten auftretenden Umwandlungsarten. Später fand man noch weitere Zerfallsarten, die nicht mehr zu diesen drei klassischen Arten gezählt werden konnten. Die Vielzahl existierender Zerfälle lässt sich in drei Kategorien einteilen:
AlphazerfallHauptartikel: Alphastrahlung
Ist der Atomkern sehr schwer, oder enthält er deutlich weniger Neutronen als Protonen, kann die Anziehung der starken Wechselwirkung überwunden werden und es kommt zum Alphazerfall. Dabei verlässt ein Helium-4-Kern, in diesem Fall Alphateilchen genannt, mit einer Geschwindigkeit von etwa 0,1 c den Mutterkern. Dies ist trotz der hohen Potentialbarriere aufgrund des Tunneleffekts möglich. Der Restkern, auch Rückstoßkern oder Tochterkern genannt, verringert bei diesem Vorgang seine Nukleonenzahl um vier und die Kernladungszahl um zwei. Beispiel für Alpha-Zerfall: Beta-ZerfallHauptartikel: Betastrahlung Wenn ein ungünstiges Verhältnis von Neutronen zu Protonen besteht, tritt normalerweise Betazerfall ein. β−-Zerfall
Beim β−-Zerfall wird im Kern ein Neutron in ein Proton umgewandelt und ein hochenergetisches Elektron sowie ein Elektron-Antineutrino emittiert. Die Nukleonenzahl des Kerns ändert sich dabei nicht, seine Ordnungszahl erhöht sich um eins. Beispiel: Durch, je nach der β-Energie, bis zu einige Meter Luft oder z. B. eine Plexiglasschicht lässt sich die Beta-Strahlung vollständig abschirmen. Die Neutrinostrahlung ist sehr schwer nachzuweisen (und völlig unschädlich), da Neutrinos nur der schwachen Wechselwirkung unterliegen. Ein Strom von Neutrinos durchquert z. B. die gesamte Erde fast ungeschwächt.
β+-Zerfall
Beim β+-Zerfall wird im Kern ein Proton in ein Neutron und ein hochenergetisches Positron umgewandelt und ein Elektron-Neutrino emittiert. Die Nukleonenzahl des Kerns ändert sich dabei nicht, seine Ordnungszahl verringert sich um eins. Beispiel: Elektroneneinfang, ε-Zerfall
Eine andere Möglichkeit zur Umwandlung eines Protons in ein Neutron besteht darin, ein Elektron aus der Atomhülle in den Kern zu „ziehen”, dem so genannten Elektroneneinfang (englisch: electron capture, kurz EC), auch ε-Zerfall genannt. Nach der Bezeichnung der typisch betroffenen Elektronenschale, der K-Schale, wird der Elektroneneinfang auch als K-Einfang bezeichnet. Das Proton des Kerns wird in ein Neutron umgewandelt, und ein Elektronneutrino emittiert. Bei diesem Umwandlungsmechanismus ist der Kern denselben Änderungen unterworfen wie beim β + -Zerfall, die Nukleonenzahl bleibt unverändert, die Ordnungszahl verringert sich um eins. Der Elektroneneinfang konkurriert daher mit dem β + -Zerfall und wird auch als eine Variante des Betazerfalls angesehen. Da der β + -Zerfall die Energie für das emittierte Positron aufbringen muss, kommt energetisch nicht für jedes Nuklid, das mit Elektroneneinfang zerfällt, der β + -Zerfall in Frage. Da das eingefangene Elektron meist aus der innersten Elektronenschale stammt, wird in dieser ein Platz frei und Elektronen aus den äußeren Schalen rücken nach, wobei charakteristische Röntgenstrahlung emittiert wird. Beispiel: Doppelter Elektroneneinfang: Bei einigen Kernen ist ein einfacher Elektroneneinfang energetisch nicht möglich, sie können sich aber durch gleichzeitigen Einfang zweier Elektronen umwandeln. Die Halbwertszeiten derartiger Umwandlungen sind typischerweise sehr lang und konnten erst in jüngster Zeit nachgewiesen werden. Beispiel: Doppelter BetazerfallBei einigen Kernen ist ein einfacher Betazerfall energetisch nicht möglich, sie können aber unter Abstrahlung zweier Elektronen zerfallen. Derartige Zerfälle haben typischerweise sehr lange Halbwertszeiten und sind erst in jüngster Zeit nachgewiesen worden. Noch offen ist die Frage, ob beim doppelten Betazerfall stets zwei Neutrinos emittiert werden, oder ob auch ein neutrinoloser doppelter Betazerfall vorkommt. Beispiel: GammazerfallHauptartikel: Gammastrahlung
Ein γ-Zerfall (γ ist der kleine griechische Buchstabe gamma) ist möglich, wenn der Atomkern nach einem Zerfall in einem energetisch angeregten Zustand vorliegt. Beim Übergang in einen energetisch niedrigeren Zustand gibt der Atomkern durch Emission hochfrequenter elektromagnetischer Strahlung, sogenannter γ-Strahlung, Energie ab. Die Emission von Gammastrahlung verändert nicht die Neutronen- und Protonenzahl des emittierenden Kerns, es erfolgt lediglich ein Übergang zwischen zwei angeregten Kernzuständen oder einem angeregten Kernzustand und dem Grundzustand. Dies geschieht meist unmittelbar nach einem Beta- oder Alphazerfall. Zum Beispiel:
das im Bild rechts als Zerfallsschema dargestellt ist. 60Co, ein Isotop mit vielen praktischen Anwendungen, ist ein Betastrahler mit einer Halbwertszeit von 5,26 Jahren. Es zerfällt zu einem angeregten Zustand von Nickel-60, der praktisch sofort (< 1 ps) durch Gammastrahlung weiter zerfällt. Es kann aber auch sein, dass der angeregte Zustand ein Kernisomer ist, d. h., dass er eine ausreichend lange Halbwertszeit hat, die eine praktische Nutzung dieser Gammastrahlungsquelle getrennt von ihrer Erzeugung ermöglicht, wie im Beispiel: Dieses Technetium-Isotop mit einer Halbwertszeit von 6 Stunden wird in der medizinischen Diagnostik verwendet. Die Bezeichnung „Gammazerfall“ entspricht zwar der Nomenklatur, ist aber hier leicht irreführend, da es sich um keinen Zerfall handelt, sondern um eine Zustandsänderung im Atomkern. Zur Abschirmung von γ-Strahlung sind unter Umständen meterdicke Beton- oder Bleiplatten nötig, denn sie hat in Materie keine bestimmte Reichweite, sondern wird nur exponentiell abgeschwächt. Es gibt daher für jedes Abschirmmaterial eine von der Gammaenergie abhängige Halbwertsdicke. γ-Strahlung ist wie Licht elektromagnetische Strahlung, sie ist aber sehr viel energiereicher und liegt damit weit außerhalb des für das menschliche Auge sichtbaren Spektrums.
Innere Konversion
Die freiwerdende Energie beim Übergang eines Atomkerns in einen energetisch niedrigeren Zustand kann auch an ein Elektron der Atomhülle abgegeben werden. Diesen Vorgang nennt man Innere Konversion. Konversionselektronen sind im Gegensatz zu β-Teilchen monoenergetisch.
Weitere ZerfallsartenSpontane SpaltungDie spontane Spaltung ist ein weiterer radioaktiver Umwandlungsprozess, der bei besonders schweren Kernen auftritt. Der Atomkern zerfällt in zwei oder mehrere Bruchstücke. Dabei entstehen in der Regel zwei etwa gleichgroße Tochterkerne und zwei oder drei Neutronen. Es ist eine Vielzahl verschiedener Tochterkernpaare möglich, jedoch sind die Summe der Kernladungszahlen und die Summe der Massenzahlen stets gleich denen des Ursprungskerns. Beispiele:
Auch die natürlich vorkommenden Uranisotope zerfallen zu einem kleinen Teil durch spontane Spaltung.
Spontane Nukleonenemission
Bei Kernen mit besonders hoher oder besonders geringer Neutronenzahl kann es zu spontaner Nukleonenemission, also Protonen- oder Neutronenemission kommen. Atomkerne mit sehr hohem Protonenüberschuss können ein Proton abgeben, Atomkerne mit hohem Neutronenüberschuss können Neutronen abgeben. 5He → 4He + 1n 9B → 8Be + 1p
ClusterzerfallStatt einzelner Nukleonen oder Helium-4-Kerne werden in sehr seltenen Fällen auch größere Atomkerne emittiert. Beispiele:
Zwei-Protonen-ZerfallBei extremem Protonenüberschuss (wie zum Beispiel bei 45Eisen) kann der Zwei-Protonen-Zerfall auftreten, bei dem sogar zwei Protonen gleichzeitig abgestrahlt werden. 45Fe → 43Cr + 2 1p
Übersicht
Größen und MaßeinheitenAktivität
Als Aktivität bezeichnet man die Anzahl der Zerfallsereignisse pro Zeiteinheit, die in einer Probe eines radioaktiven oder radioaktiv kontaminierten Stoffes auftritt.
EnergiedosisAls Energiedosis (kurz Dosis) bezeichnet man die von einem bestrahlten Objekt, z. B. Körpergewebe, über einen Belastungszeitraum absorbierte massenspezifische Energiemenge. Sie ist abhängig von der Intensität der Bestrahlung, der Absorptionsfähigkeit des bestrahlten Stoffes für die gegebene Strahlungsart und -Energie und geometrischen Faktoren.
IonendosisDie Ionendosis ist ein Maß für die Stärke der Ionisierung, ausgedrückt durch die freigesetzte Ladung pro Kilogramm des bestrahlten Stoffes.
ÄquivalentdosisDie Äquivalentdosis ist ein Maß für die Stärke der biologischen Wirkung einer bestimmten Strahlendosis. Gleich große Äquivalentdosen sind somit unabhängig von der Strahlenart in ihrer Wirkung auf den Menschen vergleichbar. Die Äquivalentdosis ergibt sich durch Multiplikation der Energiedosis (Gray) mit einem Qualitätsfaktor, der sog. Relativen biologischen Wirksamkeit, die von der Strahlungsart und -Energie abhängt und auf Erfahrungswerten beruht. Für β- und γ-Strahlung ist der Qualitätsfaktor 1, das heißt 1 Sv = 1 Gy. Für Neutronen beträgt er 10, für α-Strahlung ist er 20, was die erhöhte Wechselwirkung beim Durchdringen von Gewebe berücksichtigt.
AnwendungenTechnische AnwendungEine technische Anwendung ist die Dickenmessung und Materialprüfung mittels Durchstrahlung. Hierbei wird ein Material (mit Gamma-Strahlen) bestrahlt und ein Zähler ermittelt aufgrund der durchdringenden Strahlen und des Absorptionsgesetzes die mittlere Dichte (bei bekannter Schichtdicke) oder die Schichtdicke bei bekannter Dichte. Die Strahlung kann auch auf einem Röntgenfilm hinter der Materialschicht ein Bild erzeugen. In dieser Form wird die Durchstrahlungsprüfung bei Werkstoffen angewandt. Es wurden auch Blitzableiter mit radioaktiven Material hergestellt, deren Wirksamkeit aber nie bewiesen werden konnte (Radioaktiver Blitzableiter). Medizinische AnwendungIn der Nuklearmedizin findet man die Szintigrafie. Dabei werden geringe Mengen eines radioaktiven Stoffes in den Körper injiziert (meist γ-Strahler). Dieser Stoff strahlt dann aus dem Körper heraus, dadurch wird eine Untersuchung möglich. Die Strahlen werden von einem Detektor aufgefangen und mittels einer Gammakamera oder eines Computertomografen bildlich dargestellt. Für jedes Organ gibt es spezielle radioaktive Verbindungen. So injiziert man zum Beispiel radioaktives Iod, das sich in der Schilddrüse anlagert, um sie untersuchen zu können. (Aufgrund der Strahlenbelastung wird diese Methode heute nur noch zur Tumorbekämpfung angewandt). Weitere bildgebende Verfahren, die Radioaktivität nutzen, sind die Positronen-Emissions-Tomografie (PET) und die Single Photon Emission Computed Tomography (SPECT). Ein weiteres Einsatzfeld ist die Radionuklidbehandlung zur Schmerzlinderung bei Knochenmetastasen. Hier wird in krankhaften Knochenbereichen der Metastase ein Radionuklid angereichert, was eine schmerzlindernde Wirkung hat. Diese Methoden haben auch ein gewisses Risiko, da auch gesundes Gewebe zerstört werden kann, was zu einer Immunschwächung oder Funktionsstörung des Knochenmarks führen kann. Biologische WirkungDer Mensch kann ionisierende Strahlung, ob aus radioaktiven oder anderen Quellen, nicht direkt wahrnehmen. Für einen wirksamen Strahlenschutz beim Umgang mit radioaktiven Materialien ist daher besondere Sorgfalt und ggf. der Einsatz von Messeinrichtungen (Dosimetern) erforderlich. Hinsichtlich der Gefährlichkeit von Radioaktivität müssen zwei verschiedene Risiken unterschieden werden: 1. die Strahlenbelastung selbst, 2. die Kontamination (Verunreinigung) mit radioaktivem Material, die unter Umständen zu lange andauernder Bestrahlung führen kann, insbesondere z. B. bei Kontamination der Haut von Personen oder gar Aufnahme (Inkorporation) radioaktiver Substanz in den Körper durch Einatmen (Inhalation) oder Essen/Trinken (Ingestion). Diese beiden Begriffe werden in Berichterstattung und Öffentlichkeit oft verwechselt. Entsprechend wird beispielsweise der Begriff „verstrahlt“ falsch anstatt kontaminiert benutzt; Verstrahlung bedeutet – analog der Verbrennung – eine durch Bestrahlung hervorgerufene erhebliche Schädigung oder Verletzung. Die Strahlenbelastung für Lebewesen wird als effektive Dosis oder Äquivalentdosis in der Einheit Sievert gemessen (s. oben). Darin wird die unterschiedliche Schädlichkeit von α-,β- und γ-Strahlen sowie die unterschiedliche Empfindlichkeit einzelner Gewebe berücksichtigt. Die Alphastrahlung hat auf lebendes Gewebe durch ihre Ionisierungsfähigkeit eine besonders hohe schädliche Wirkung, jedoch besitzt sie in Luft eine Reichweite von nur wenigen Zentimetern und kann durch ein einfaches Blatt Papier vollständig abgeschirmt werden (den gleichen Zweck erfüllen die obersten abgestorbenen Hautschuppen), so dass Alphastrahler, die sich außerhalb des menschlichen Körpers befinden, weitgehend ungefährlich sind. Gefährlich sind Alphastrahler, wenn sie in direkten Kontakt mit lebendem Gewebe kommen. Ein Weg dafür ist das Einatmen von Aerosolen, die über die Schleimhäute des Atemweges aufgenommen werden; radioaktiver Staub wird in der Lunge eingelagert und kann dort Krebs auslösen. Das Edelgas Radon wird zwar nicht eingelagert, gefährdet aber während des Einatmens durch Zerfälle in der Lunge. Wenn ein Alphastrahler mit einer Halbwertszeit von einigen Tagen durch Nahrung aufgenommen wurde oder durch Injektion in den Blutkreislauf gebracht wurde, können bereits wenige Mikrogramm für Menschen tödlich sein. Unmittelbar beobachtbare (akute) Strahlenwirkungen (Strahlenkrankheit) treten beim Menschen erst bei sehr hohen kurzfristigen Äquivalentdosen ab 0,5 Sv auf. Auch wesentlich geringere Strahlendosen führen jedoch mit einer gewissen Wahrscheinlichkeit zu Langzeitfolgen (Krebs oder Erbschäden). Anderseits ist es bemerkenswert, dass beispielsweise Bad Gastein ein seit dem Mittelalter berühmtes Heilbad ist, dessen Heilwasser sich lediglich durch hohe Temperatur und den Gehalt an Radon auszeichnet, siehe Radonbalneologie. Natürliche StrahlenbelastungJeder Mensch ist natürlicher Strahlenbelastung ausgesetzt. Ein kleiner Teil davon geht auf ständig vorhandene Radionuklide im eigenen Körper zurück (beim Erwachsenen rund 8000 Bq, hauptsächlich Kohlenstoff-14 und Kalium-40). Die übrige, äußere natürliche Strahlenbelastung stammt etwa zur Hälfte von aus dem Erdboden austretendem Radon und seinen Zerfallsprodukten, daneben auch von Kalium-40 in Baustoffen und einigen anderen Nukliden. Radon ist als die zweithäufigste Ursache für Lungenkrebs in Deutschland bezeichnet worden. WarnzeichenHauptartikel: Trefoil, ISO 21482 Weil das bisher verwendete Warnzeichen (☢, Trefoil genannt, im Unicode an Code-Position U+2622) oft nicht als Warnung vor starken radioaktiven Strahlern erkannt wurde, kam es vor allem in Entwicklungsländern schon zu tödlichen Unfällen, weil Menschen ein stark strahlendes Nuklid aus seiner Abschirmung entnahmen (zum Beispiel der Goiânia-Unfall in Brasilien im Jahr 1987). Am 15. Februar 2007 gab deshalb die IAEA bekannt, dass direkt an Nukliden der Strahlungskategorie 1, 2 und 3 [1] ein neues, auffälligeres Warnschild angebracht werden soll. Dieses warnt mit Hilfe von aussagekräftigen Symbolen vor der tödlichen Gefahr durch radioaktive Strahlung und fordert zur Flucht auf. Am Behälter selbst soll weiterhin nur das alte Symbol angebracht werden, da er die Strahlung soweit abschirmt, dass sie keine unmittelbare Gefahr darstellt. Durch die Normung als ISO Norm 21482 soll das neue Warnschild für gefährliche Strahlenquellen möglichst schnell und international verbindlich eingeführt werden. Bei schwachen Strahlenquellen soll keine Änderung der Kennzeichnung erfolgen. [2] Siehe auchQuellenKategorien: Radioaktivität | Kernphysik |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dieser Artikel basiert auf dem Artikel Radioaktivität aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||





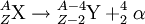
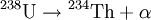
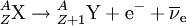
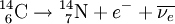
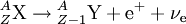
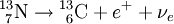
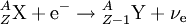
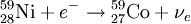
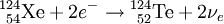
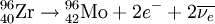
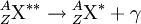
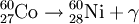 ,
,