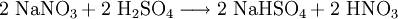Um alle Funktionen dieser Seite zu nutzen, aktivieren Sie bitte die Cookies in Ihrem Browser.
my.chemie.de
Mit einem my.chemie.de-Account haben Sie immer alles im Überblick - und können sich Ihre eigene Website und Ihren individuellen Newsletter konfigurieren.
- Meine Merkliste
- Meine gespeicherte Suche
- Meine gespeicherten Themen
- Meine Newsletter
Salpetersäure
Salpetersäure (nach der Nomenklatur der IUPAC Hydrogennitrat genannt) ist die bekannteste und stabilste Sauerstoffsäure des Stickstoffs. Der Name leitet sich vom Salpeter ab, aus dem sie durch Zugabe einer stärkeren Säure (Salzsäure, Schwefelsäure) gewonnen werden kann. Salpetersäure liegt in wässriger Lösung weitgehend dissoziiert vor. Als starke anorganische Säure zählt sie zu den Mineralsäuren. Ihre Salze und Ester heißen Nitrate. Die Salze werden auch mit dem Trivialnamen „-salpeter“ gekennzeichnet, z. B.: Chilesalpeter, (Kali-)Salpeter, Ammonsalpeter, Kalksalpeter, Barytsalpeter, Mauersalpeter etc. Weiteres empfehlenswertes Fachwissen
GeschichteIn der Schrift De inventione veritatis aus dem 12. Jahrhundert wird erwähnt, dass bereits im 9. Jahrhundert der arabische Alchimist Geber rohe Salpetersäure („Aqua dissolutiva“) durch trockenes Erhitzen von Salpeter (lat. sal petrae = Felsensalz; KNO3), Cyprischem Vitriol (CuSO4·5H2O) und Alaun (KAl(SO4)2·12H2O) gewonnen haben soll. Im 13. Jahrhundert benutzte Albertus Magnus die Salpetersäure, um Gold und Silber zu trennen („Scheidewasser“). Viele Schriften wurden Albertus Magnus irrtümlich zugeschrieben, um der Schrift höheres Gewicht zu verleihen, wahrscheinlich auch die Verwendung der Salpetersäure. Schon 1225 soll Raymund von Lullius sie fabrikmäßig durch Glühen von Salpeter mit Ton hergestellt haben, was aber vom chemischen Standpunkt unwahrscheinlich ist. Später wurde Salpeter mit Eisenvitriol (FeSO4·7H2O) erhitzt, was höhere Ausbeuten bei niedrigerer Temperatur lieferte. J. R. Glauber gewann Mitte des 17. Jahrhunderts reinen spiritus nitri durch Umsetzung und Destillation von Salpeter mit Schwefelsäure, einem bis heute gebräuchlichen Laborverfahren zur Herstellung der Salpetersäure, die im Mittelalter auch aqua fortis oder aqua valens und im englischen Sprachraum strong water genannt wurde. Als Bestandteile der Salpetersäure erkannte A. L. Lavoisier Mitte des 18. Jahrhunderts die chemischen Elemente Stickstoff und Sauerstoff. Die genaue Zusammensetzung wurde von Henry Cavendish bestimmt, dem auch die Synthese aus dem Stickstoff der Luft durch elektrische Entladung gelang. Eine rationelle Fabrikation begann erst Anfang des 19. Jahrhunderts, als billige Schwefelsäure und Chilesalpeter in ausreichenden Mengen verfügbar waren. Auch die „Luftverbrennung“ in einem elektrischen Lichtbogen wurde zu einem großtechnischen Verfahren entwickelt (Birkeland–Eyde), das jedoch nur in Ländern mit billigem Strom konkurrenzfähig war. Die Katalytische Oxidation von Ammoniak über Platin wurde von C. F. Kuhlmann (1838) entdeckt. Bis zur Erfindung der Ammoniaksynthese durch Haber und Bosch blieb jedoch Ammoniak zu teuer im Vergleich zu Chilesalpeter. Zu Beginn des 20. Jahrhunderts entwickelte Wilhelm Ostwald die Herstellung von Salpetersäure aus Ammoniak zur industriellen Reife. Die billige Ammoniak-Oxidation hat heute alle anderen großtechnischen Verfahren verdrängt. HerstellungSalpetersäure wird technisch seit 1908 nach dem Ostwaldverfahren hergestellt. Es handelt sich dabei um die katalytische Oxidation von Ammoniak. Das Ammoniak-Luft-Gemisch wird rasch (1/1000 s Berührungszeit) durch heiße Platin-Rhodium-Netze (Katalysator) geleitet. Bei 800 °C entsteht Stickstoffmonoxid, das beim Abkühlen mit überschüssigem Sauerstoff zu Stickstoffdioxid und dann in Rieseltürmen mit Wasser zu etwa 60%iger Salpetersäure reagiert. Die 60%ige Salpetersäure kann durch Destillation bis 68 % konzentriert werden, was dem Azeotrop mit Siedepunktmaximum (122 °C) entspricht. Höhere Konzentrationen lassen sich durch Entwässerung mit Magnesiumnitrat (Mg(NO3)2) oder durch Behandlung von Distickstofftetraoxid (N2O4) mit der stöchiometrisch nötigen Menge von Luft und Wasser erreichen. Im Labormaßstab kann rauchende Salpetersäure durch Umsetzung konzentrierter Schwefelsäure mit Alkalinitraten dargestellt werden. Vor 1908 wurde Salpetersäure durch dieses Verfahren unter Verwendung von Natriumnitrat (Chilesalpeter) gewonnen. Eigenschaften
Salpetersäure ist in reinem Zustand farblos. Konzentrierte Salpetersäure zersetzt sich jedoch leicht (besonders unter Lichteinwirkung) und hat aufgrund des in ihr gelösten Stickstoffdioxids (NO2) oft einen gelblichen oder rötlichen Farbton. Reine Salpetersäure, die freies Stickstoffdioxid enthält, wird rauchende Salpetersäure genannt. Sie enthält über 90 % HNO3 und wirkt stark oxidierend und kann manche leicht brennbaren Stoffe entzünden. Salpetersäure, die durch gelöstes Stickstoffdioxid gelb gefärbt ist, kann durch eine kleine Menge Harnstoff oder besser Harnstoffnitrat entfärbt werden. Salpetersäure löst die meisten Metalle auf. Ausnahmen sind die Edelmetalle Gold, Platin und Iridium. Auch Aluminium, Titan, Zirconium, Hafnium, Niob, Tantal und Wolfram widerstehen in Folge der Passivierung durch Salpetersäure, wobei sich auf dem Metall eine fest haftende, undurchlässige Oxidschicht bildet. Da man somit Gold und Silber trennen konnte, wurde sie früher Scheidewasser genannt. Gemischt mit Salzsäure (Königswasser) kann sie auch diese Edelmetalle auflösen. Weiter sind Aluminium und Eisen infolge Passivierung resistent gegenüber kalter, Chrom gegenüber heißer Salpetersäure. Beim Kontakt von Eiweißen, die aromatische Aminosäuren wie L-Phenylalanin oder L-Tyrosin enthalten werden diese von der Salpetersäure unter Nitrierung des Benzolrings gelbgefärbt. Die Reaktion wird Xanthoprotein-Reaktion genannt und kann zum Nachweis Aromatischer Aminosäuren bzw. von Eiweißen benutzt werden.
Physikalische Eigenschaften von HNO3/H2O-Mischungen in Abhängigkeit von der Konzentration bei 20 °C und 1,013 bar
VerwendungSalpetersäure ist einer der wichtigsten Grundstoffe der chemischen Industrie. Sie dient:
Gemische mit Schwefelsäure (zwei Teile Schwefelsäure und ein Teil Salpetersäure) werden Nitriersäure genannt und zur Nitrierung von organischen Verbindungen verwendet. Sie wurde bis in die späten 1980er Jahre in der Raketentechnik als Oxidator verwendet (z. B. in der Agena-Oberstufe). Da Salpetersäure die Aminogruppen in den Basen (Adenin, Thymin, Guanin, Cytosin) der DNA zu Hydroxyl-Gruppen umwandeln kann, wird sie neuerdings dazu benutzt, um Mutationen in der DNA zu erzeugen. Aufgrund dieser Eigenschaft der Salpetersäure gilt sie als krebserregend. NachweisSalpetersäure kann mittels Nitratnachweis durch die Ringprobe und durch Lunges Reagenz nachgewiesen werden. Diese Nachweisverfahren werden auch als klassische Verfahren bezeichnet. Siehe auchQuellen
Kategorien: Brandfördernder Stoff | Ätzender Stoff | Mineralsäure | Stickstoffverbindung | Nitrat |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dieser Artikel basiert auf dem Artikel Salpetersäure aus der freien Enzyklopädie Wikipedia und steht unter der GNU-Lizenz für freie Dokumentation. In der Wikipedia ist eine Liste der Autoren verfügbar. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||